Para compreender a verdadeira profundidade da Psiconeuroimunoendocrinologia, é necessário abandonar definitivamente a herança do dualismo cartesiano que separou, por séculos, a mente do corpo. O estudante ou profissional de saúde que deseja mergulhar neste universo não pode mais olhar para o paciente como uma coleção de órgãos isolados que ocasionalmente interagem. É preciso enxergar o paciente como um ecossistema complexo, um holobionte multiespécies, no qual trilhões de bactérias, circuitos neuronais, cascatas endócrinas e legiões de células imunológicas operam sob uma única rede de sinalização molecular contínua e não hierárquica. O sistema imunológico, neste cenário, transcende sua função clássica de defesa bélica contra patógenos. Ele atua como um órgão sensorial difuso e altamente sofisticado, capaz de detectar ameaças que escapam aos nossos cinco sentidos clássicos — desde a invasão de um vírus até a toxicidade de um estresse psicossocial crônico, um trauma de infância ou a qualidade da nossa dieta. Mergulhemos nos mecanismos moleculares finos que governam esta sinfonia biológica, onde a alteração em um único acorde bioquímico pode ecoar na forma de psicose, depressão ou neurodegeneração.
A Arquitetura da Sinalização Neuroimune e o Nervo Vago
A comunicação entre o microambiente periférico e o parênquima cerebral ocorre de forma ininterrupta e simultânea por meio de vias humorais e neurais. Na via humoral, citocinas pró-inflamatórias primárias, como a Interleucina-1 beta (IL-1β), a Interleucina-6 (IL-6) e o Fator de Necrose Tumoral alfa (TNF-α), circulam pelo sangue e alcançam o cérebro. Como a barreira hematoencefálica impede a passagem livre dessas macromoléculas, elas utilizam transportadores ativos específicos ou penetram pelas janelas do cérebro, os órgãos circunventriculares, que são desprovidos de uma barreira estrita. Ao atingirem as células endoteliais cerebrais, essas citocinas induzem a produção de prostaglandinas (especialmente PGE2), que se difundem para o tecido neural. Contudo, a via mais fascinante e rápida de comunicação é a neural, protagonizada pelo nervo vago. As fibras aferentes vagais que inervam as vísceras estão repletas de receptores para citocinas e metabólitos bacterianos. Quando uma tempestade inflamatória ocorre no intestino ou no fígado, o nervo vago capta essa informação química e a converte em potenciais de ação (sinais elétricos) que viajam em milissegundos até o núcleo do trato solitário no tronco encefálico. A partir daí, a informação é retransmitida para o sistema límbico, alterando quase instantaneamente a percepção de segurança e o estado motivacional do indivíduo. Em contrapartida, o cérebro tenta modular essa inflamação periférica através do reflexo inflamatório vagal. Fibras eferentes disparam sinais de volta ao baço e ao intestino, liberando o neurotransmissor acetilcolina. A acetilcolina se liga aos receptores nicotínicos alfa-7 (α7nAChR) presentes na superfície dos macrófagos, bloqueando a ativação do fator de transcrição NF-κB e freando a produção de citocinas. Este é o controle da mente sobre a imunidade; contudo, sob estresse severo ou trauma, este tônus vagal desaba, deixando a inflamação correr solta.
O Eixo HPA, o Paradoxo do Cortisol e a Inflamação Estéril
Para compreender o impacto dos estressores psicossociais, é imperativo desvendar o papel dúbio do cortisol. Quando o cérebro percebe uma ameaça ambiental (uma humilhação pública, luto, violência ou insegurança financeira persistente), o hipotálamo libera CRH, que estimula a pituitária a secretar ACTH, que por sua vez sinaliza para as glândulas adrenais liberarem cortisol e catecolaminas (adrenalina e noradrenalina). Fisiologicamente, o cortisol é o maior imunossupressor e anti-inflamatório endógeno que possuímos. Ele entra nas células imunes, liga-se ao seu receptor citoplasmático e desliga a transcrição de genes pró-inflamatórios. Portanto, um estresse agudo deveria suprimir a imunidade. O paradoxo biológico ocorre na cronicidade. A exposição ininterrupta ao estresse psicossocial mantém os níveis de cortisol perenemente elevados. Para se proteger dessa inundação hormonal, as células imunológicas, especialmente os monócitos e macrófagos, realizam uma regulação negativa de seus receptores, um fenômeno conhecido como Resistência aos Glicocorticoides. A partir deste momento, as células de defesa ficam “surdas” ao cortisol. Sem este freio natural, o sistema imune fica hiper-reativo.
Simultaneamente, o estresse crônico gera dano tecidual microscópico que libera moléculas de dentro das células humanas, como o ATP extracelular e as proteínas de choque térmico (HSPs). Estas moléculas são chamadas de DAMPs (Padrões Moleculares Associados ao Dano). Os receptores da imunidade inata, notadamente o Toll-Like Receptor 4 (TLR4), não sabem distinguir se o dano veio de uma bactéria ou de um trauma psicológico. A ligação dos DAMPs ao TLR4 inicia uma inflamação estéril. Dentro da célula imune, ativa-se um maquinário enzimático complexo chamado Inflamassoma NLRP3, que cliva a pro-IL-1β, transformando-a em uma citocina madura e ativa que é secretada para a corrente sanguínea. O paciente, portanto, experimenta um incêndio bioquímico sem ter nenhuma infecção, gerado exclusivamente pela carga alostática do seu sofrimento psíquico.
O Sequestro do Triptofano e a Gênese Neuroquímica da Depressão
A inflamação crônica de baixo grau não permanece na periferia; ela invade a neuroquímica, reescrevendo as bases biológicas da psiquiatria. Historicamente, a depressão foi tratada apenas como uma deficiência na fenda sináptica de neurotransmissores como a serotonina. O olhar psiconeuroimunológico revela o porquê dessa deficiência. Durante um estado inflamatório (seja por obesidade, disbiose, doenças autoimunes ou estresse psicossocial), o fígado, as células endoteliais cerebrais e a própria microglia aumentam exponencialmente a expressão de uma enzima chamada IDO (indoleamina 2,3-dioxigenase). A enzima IDO tem uma avidez imensa pelo triptofano, que é o aminoácido precursor da serotonina. Ela literalmente “rouba” o triptofano do cérebro e o desvia para uma rota metabólica destrutiva conhecida como a Via da Cinurenina.
Ao reduzir a disponibilidade de triptofano, a produção de serotonina e melatonina desaba, explicando a tristeza e a insônia severa. Mas o quadro é ainda mais sombrio. A cinurenina atravessa a barreira hematoencefálica e, dentro do cérebro, é metabolizada pela microglia hiperativada em Ácido Quinolínico. O ácido quinolínico é uma potente neurotoxina e um agonista dos receptores NMDA do glutamato. Sua presença inunda os neurônios com cálcio, causando estresse oxidativo, excitotoxicidade glutamatérgica e, em última instância, apoptose (morte celular) em áreas nobres como o hipocampo e o córtex pré-frontal. Além disso, a inflamação suprime a transcrição do BDNF (Fator Neurotrófico Derivado do Cérebro), paralisando a neurogênese e a capacidade do cérebro de formar novas sinapses. A depressão resistente ao tratamento, portanto, não é uma falha psicológica do paciente; é o resultado de uma toxicidade metabólica na qual o cérebro está literalmente sofrendo atrofia devido ao bombardeio imune.
A Imunidade Treinada e a Memória Epigenética do Trauma
O dogma central da imunologia ditava que apenas linfócitos T e B possuíam memória celular. Hoje, a ciência nos mostra que a imunidade inata (macrófagos e microglias) possui um diário molecular de tudo o que vivemos, um fenômeno chamado Imunidade Treinada. Quando um indivíduo passa por experiências adversas na infância (ACEs), como abuso, negligência severa ou infecções graves precoces, o banho de catecolaminas e citocinas atinge diretamente a medula óssea. Lá, as células-tronco que dão origem aos glóbulos brancos sofrem uma reprogramação epigenética profunda. Enzimas modificam a estrutura da cromatina (o carretel onde o DNA é enrolado), mantendo os genes pró-inflamatórios em um estado constantemente “desenrolado” e acessível.
Em termos de metabolismo intracelular, ocorre o Efeito Warburg, onde a célula abandona a via respiratória normal e passa a usar a glicólise aeróbica rápida, preparando-se para a guerra contínua. O resultado é trágico: essas células imunes, e suas descendentes por décadas, já nascem com um limiar de reatividade baixíssimo. Na vida adulta, diante de um estressor corriqueiro do ambiente de trabalho, o sistema imune inato responde com uma tempestade de citocinas desproporcional. No sistema nervoso central, a microglia passa pelo mesmo processo, tornando-se “primada”. O trauma não é apenas uma lembrança dolorosa retida na circuitaria psicológica; é uma configuração física e molecular no epigenoma da medula óssea e das células gliais do paciente.
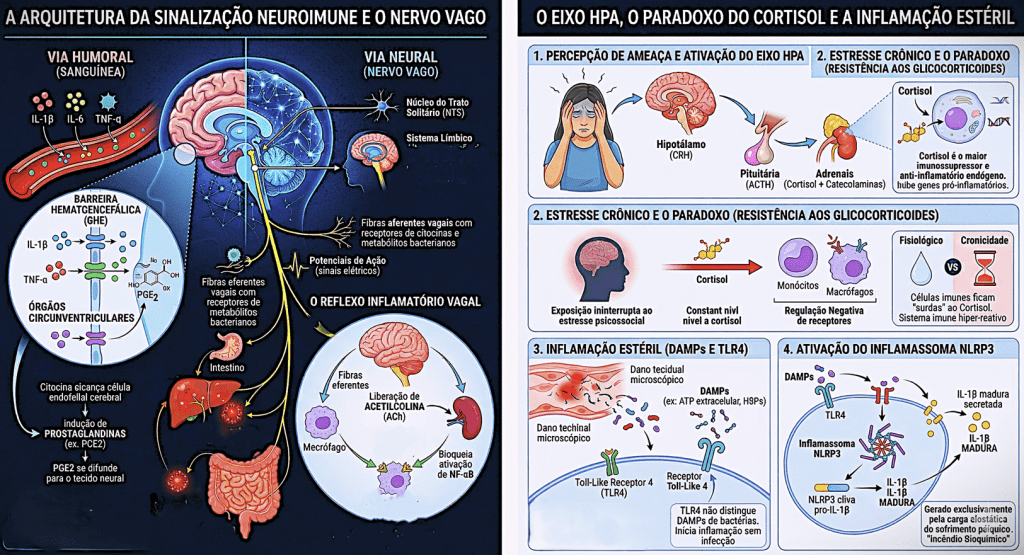
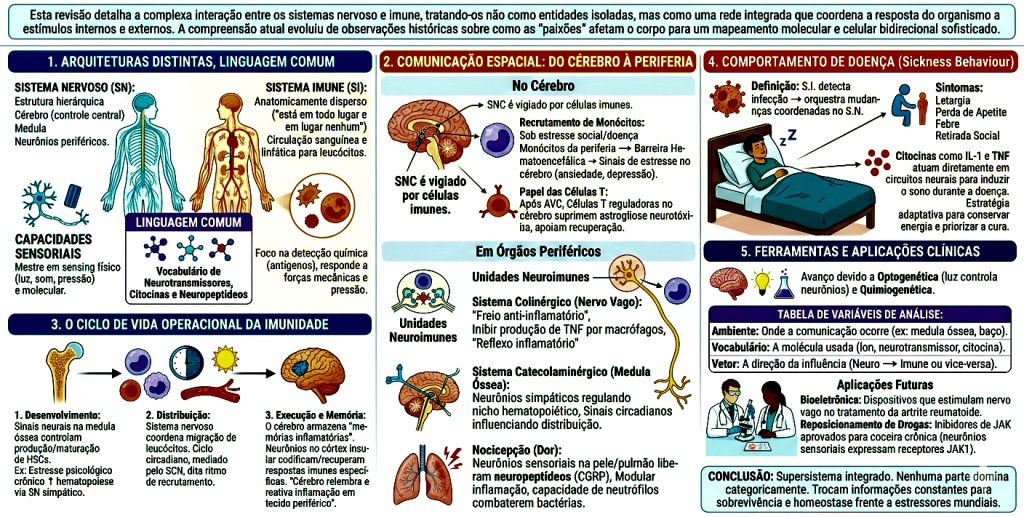
Para compreender a profunda conexão entre a mente e o corpo, o infográfico detalha as vias de comunicação neuroimunes e os mecanismos pelos quais o estresse psicológico crônico se materializa em inflamação física estrutural. Essa comunicação ocorre de duas maneiras principais. Pela via humoral, citocinas inflamatórias como IL-1β, IL-6 e TNF-α viajam pela corrente sanguínea e interagem com a barreira hematoencefálica e os órgãos circunventriculares. Essa interação induz as células endoteliais a produzirem prostaglandinas, a exemplo da PGE2, que se difundem para o tecido neural e alteram o funcionamento cerebral. Simultaneamente, a via neural atua como uma via expressa de comunicação bidirecional através do nervo vago. Fibras aferentes detectam citocinas e metabólitos no intestino, enviando sinais elétricos rápidos para o sistema límbico no cérebro. Em resposta, o corpo utiliza o “reflexo inflamatório vagal” como um freio natural: o cérebro envia sinais de volta que liberam acetilcolina, bloqueando a ativação do fator NF-κB nos macrófagos e inibindo o processo inflamatório perifericamente.
A complexidade dessa rede se torna evidente quando analisamos a cascata do estresse. Inicialmente, a percepção de uma ameaça psicológica ativa o eixo HPA (Hipotálamo-Pituitária-Adrenal), culminando na liberação de cortisol, que em seu estado fisiológico normal é o nosso maior imunossupressor e anti-inflamatório endógeno. No entanto, a exposição ininterrupta ao estresse psicossocial cria um cenário crônico que gera o “paradoxo da resistência aos glicocorticoides”. Com os níveis de cortisol constantemente elevados, células imunes como monócitos e macrófagos sofrem uma regulação negativa em seus receptores. Na prática, essas células ficam “surdas” ao cortisol, tornando o sistema imunológico hiper-reativo e persistentemente inflamado, mesmo banhado por este hormônio.
Esse estado de hiper-reatividade abre caminho para a chamada inflamação estéril. O estresse crônico e os consequentes danos celulares microscópicos liberam moléculas de sinalização de perigo conhecidas como DAMPs, como o ATP extracelular. Os receptores imunológicos Toll-Like 4 (TLR4) identificam essas moléculas, mas são incapazes de distingui-las de bactérias invasoras reais. Consequentemente, iniciam uma forte resposta inflamatória na ausência de qualquer infecção. Essa sinalização engatilha o inflamassoma NLRP3, um complexo celular que passa a clivar moléculas precursoras e secretar a citocina IL-1β madura. O resultado final dessa cascata é um verdadeiro “incêndio bioquímico”, uma inflamação sistêmica e cerebral gerada e sustentada exclusivamente pela carga alostática do sofrimento psíquico.
O Eixo Microbiota-Intestino-Cérebro e a Perda da Barreira
A individualidade humana é uma ilusão biológica. O intestino abriga trilhões de microrganismos que ditam as regras da nossa tolerância imunológica e do nosso humor. Em um estado de simbiose saudável (eubiose), bactérias específicas fermentam as fibras da nossa dieta e produzem Ácidos Graxos de Cadeia Curta (AGCCs), especialmente o Butirato. O butirato atua como um maestro da paz: ele fortalece as tight junctions (junções de oclusão) que colam uma célula intestinal na outra, e atua nas células dendríticas forçando a maturação de Linfócitos T Reguladores (Tregs), que são os soldados que promovem a tolerância e silenciam autoimunidades. Além disso, o butirato cai na corrente sanguínea, atravessa a barreira hematoencefálica e age epigeneticamente inibindo histonas desacetilases na microglia, promovendo um estado de neuroproteção.
No entanto, a vida moderna — caracterizada por dietas ultraprocessadas, uso indiscriminado de antibióticos e estresse psicossocial extremo — aniquila a diversidade dessa microbiota. A disbiose resultante promove a Síndrome do Intestino Permeável. A barreira física se rompe, e fragmentos das membranas de bactérias mortas, o Lipopolissacarídeo (LPS), translocam massivamente para o sangue. Esse fenômeno, chamado de endotoxemia metabólica, enlouquece o sistema imunológico sistêmico. O LPS viaja até o cérebro, ativando receptores nas células endoteliais da barreira hematoencefálica e tornando-a também porosa. Infiltrados inflamatórios entram no parênquima neural, alterando a síntese de dopamina e GABA. A patologia muitas vezes nasce no intestino e migra para a mente. O Parkinson, por exemplo, não começa com tremores; a hipótese de Braak sugere que proteínas alfa-sinucleínas se dobram erroneamente no sistema nervoso entérico devido à inflamação intestinal crônica, viajando retrogradamente pelo nervo vago durante décadas até atingir a substância negra do mesencéfalo.
Doenças Imunomediadas, Mastócitos e a Ruptura da Tolerância
Quando os mecanismos regulatórios, como as células Treg instruídas pelo intestino, falham, o holobionte se volta contra si mesmo. A psiquiatria está passando por uma revolução ao descobrir que muitos quadros agudos de psicose, catatonia e delírios não são esquizofrenia clássica, mas sim Encefalites Autoimunes. O exemplo paradigmático é a encefalite anti-NMDAR. Por uma quebra na tolerância dos linfócitos B (muitas vezes desencadeada por um teratoma ovariano ou uma infecção viral cruzada), o corpo produz anticorpos contra os próprios receptores NMDA dos neurônios do córtex e do hipocampo. Os anticorpos forçam o neurônio a “engolir” seus próprios receptores, gerando um apagão glutamatérgico massivo. O paciente enlouquece, mas o defeito não é psiquiátrico na origem; é um ataque imunológico focado, tratável não com antipsicóticos, mas com plasmaférese e imunossupressão.
Da mesma forma, não podemos ignorar a hipersensibilidade. O paciente atópico (alérgico crônico) possui um sistema imune polarizado para Th2. O que poucos sabem é que os mastócitos — as células que armazenam histamina — não estão apenas na pele ou no nariz; eles formam sentinelas ao redor dos vasos sanguíneos cerebrais, no tálamo e na dura-máter. Estressores emocionais agudos liberam Hormônio Liberador de Corticotrofina (CRH) diretamente nos mastócitos cerebrais, induzindo sua degranulação explosiva sem a presença de nenhum alérgeno físico. A histamina e a triptase liberadas no cérebro geram edema vascular focal, névoa mental profunda (brain fog) e crises de ansiedade aguda, uma vez que a histamina central é um potente neurotransmissor excitatório. A alergia e a hiper-reatividade emocional compartilham a exata mesma via molecular.
Inflammaging, Obesidade e a Lenta Erosão Neurodegenerativa
À medida que o corpo envelhece, as agressões ao DNA, o encurtamento dos telômeros e o estresse oxidativo fazem com que células de múltiplos tecidos parem de se dividir e entrem em senescência. Essas “células zumbis” não morrem, mas adquirem um fenótipo secretor associado à senescência (SASP), expelindo continuamente um coquetel letal de citocinas e metaloproteinases que destroem o tecido circundante. O sistema imunológico do idoso, exausto e focado em manter vírus latentes como o Citomegalovírus sob controle, falha em limpar essas células zumbis. Instala-se o “Inflammaging” (Envelhecimento Inflamatório), o motor oculto do Alzheimer e do declínio cognitivo. A microglia senescente perde a capacidade de fagocitar as placas de beta-amiloide e, em vez disso, ataca as sinapses saudáveis.
Esse processo é drasticamente acelerado pelo sedentarismo e pela obesidade. O tecido adiposo visceral da síndrome metabólica é uma bomba-relógio imunológica. Adipócitos hipertrofiados sofrem hipóxia, morrem e atraem macrófagos formadores de coroa. Essa gordura inflamada lança TNF-α e resistina no sangue, promovendo resistência insulínica periférica e central. Quando o cérebro se torna resistente à insulina, os neurônios perdem a capacidade de captar glicose, sofrendo fome metabólica e morte acelerada (o que muitos cientistas chamam de Diabetes Tipo 3). Paralelamente, o sedentarismo priva o cérebro das miocinas (como a irisina e a interleucina-6 em pulso agudo) que os músculos esqueléticos em contração liberam, que são os maiores reparadores neurais e fatores antienvelhecimento conhecidos.
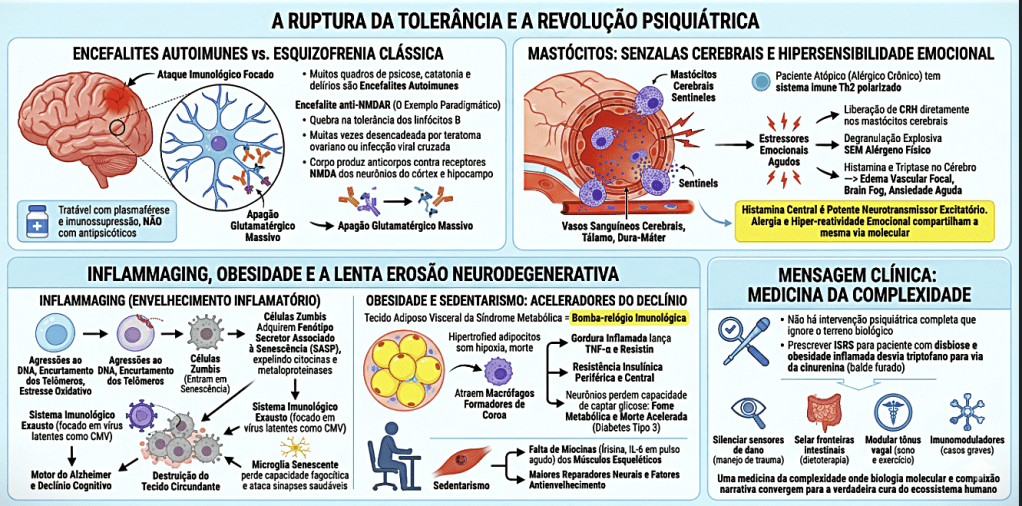
A revolução psiquiátrica contemporânea propõe uma mudança de paradigma ao analisar a ruptura da tolerância imunológica como causa central de transtornos mentais. O infográfico demonstra que a fronteira entre a neurologia e a psiquiatria é tênue, revelando que muitos quadros diagnosticados como esquizofrenia clássica, psicose ou catatonia são, na verdade, encefalites autoimunes. O exemplo paradigmático é a encefalite anti-NMDAR, onde uma quebra na tolerância dos linfócitos B — muitas vezes desencadeada por infecções ou tumores — leva o corpo a produzir anticorpos que atacam os receptores de glutamato no córtex e hipocampo, gerando um “apagão” neuronal que não responde a antipsicóticos, mas sim a tratamentos de imunossupressão.
Paralelamente a esses ataques agudos, existe uma via de hipersensibilidade emocional mediada pelos mastócitos, as células sentinelas do cérebro. Em pacientes atópicos ou cronicamente alérgicos, o sistema imune opera em um estado polarizado. Quando esses indivíduos enfrentam estressores emocionais agudos, ocorre uma liberação de hormônios que ativam os mastócitos cerebrais, causando uma degranulação explosiva de histamina e triptase. Esse processo resulta em edema vascular focal e “brain fog”, provando que a alergia e a hiper-reatividade emocional compartilham a mesma via molecular inflamatória.
No campo do envelhecimento, o conceito de “Inflammaging” descreve a lenta erosão neurodegenerativa causada por agressões ao DNA e estresse oxidativo. Esse processo cria as chamadas “células zumbis”, que param de se dividir mas continuam expelindo citocinas tóxicas que destroem o tecido circundante e exaurem o sistema imunológico. Esse cenário é agravado pela obesidade e pelo sedentarismo; o tecido adiposo visceral atua como uma bomba-relógio imunológica, lançando gordura inflamada que gera resistência insulínica cerebral — a chamada Diabetes Tipo 3 —, onde os neurônios morrem por incapacidade de captar glicose. Sem o exercício físico para liberar miocinas protetoras, o cérebro perde sua capacidade de reparo.
A conclusão clínica dessa medicina da complexidade é que nenhuma intervenção psiquiátrica é completa se ignorar o terreno biológico. Prescrever apenas antidepressivos (ISRS) para um paciente com disbiose intestinal e obesidade é ineficaz, pois a inflamação desvia o triptofano para vias metabólicas tóxicas. A verdadeira cura do ecossistema humano exige uma abordagem integrada: silenciar os sensores de dano através do manejo de traumas, selar as fronteiras intestinais com dietoterapia, modular o sistema nervoso com sono e exercícios, e utilizar imunomoduladores quando necessário, unindo a biologia molecular à compaixão narrativa.
Para o clínico, o terapeuta e o neurocientista, a mensagem é incontornável: não há intervenção psiquiátrica completa que ignore o terreno biológico. Prescrever um inibidor de recaptação de serotonina para um paciente cuja disbiose e obesidade inflamada desviam todo o seu triptofano para a via da cinurenina é como tentar encher um balde furado. É preciso silenciar os sensores de dano da medula óssea com manejo de trauma, selar as fronteiras intestinais com dietoterapia profunda, modular o tônus vagal com regulação do sono e exercício físico, e, em casos graves, utilizar imunomoduladores. O estudo desta teia nos obriga a abandonar a especialização que cega, convidando-nos a praticar uma medicina da complexidade, onde a biologia molecular e a compaixão narrativa convergem para a verdadeira cura do ecossistema humano.
TEXTO PSICOIMUNOLOGIA – LINK DE ACESSO
https://play.google.com/store/books/details?id=NFCUEQAAQBAJ
PSCINEUROIMUNOLOGIA EM MAIORES DETALHES
O Ser Ecossistêmico e a Nova Fronteira da Mente
A compreensão do organismo humano como uma entidade biológica isolada cede espaço à caracterização do holobionte multiespécies, definindo a unidade funcional composta pelo hospedeiro e sua microbiota associada. Esta configuração pressupõe que a homeostase não depende exclusivamente de processos genômicos endógenos, integrando informações moleculares provenientes de trilhões de microrganismos que coabitam nichos específicos, especialmente o trato gastrointestinal.
A psiconeuroimunologia analisada dentro dessa perspectiva estabelece que as interações entre os sistemas nervoso, endócrino e imunológico não seguem uma hierarquia linear ou centralizada. Em vez disso, as vias de sinalização operam em uma rede de conexões múltiplas e multidirecionais, onde cada ponto de contato pode influenciar o comportamento global do sistema sem a necessidade de um comando central único. A imunologia assume o papel de um sistema sensorial complexo que monitora o estado interno e ambiental, traduzindo estímulos bioquímicos em respostas fisiológicas e comportamentais. Durante séculos, entramos nos consultórios e laboratórios carregando o peso de um dualismo silencioso. Tratamos o cérebro como um monarca isolado, uma torre de marfim que governa o corpo sem se misturar com a “plebe” orgânica. Mas a biologia molecular moderna, com sua precisão quase poética, veio derrubar esses muros. Quando olhamos para um ser humano hoje, não vemos mais um indivíduo isolado; vemos um Holobionte.
Imagine-se não como uma unidade fechada, mas como um ecossistema pulsante. Não somos apenas o resultado dos nossos genes humanos; somos uma unidade funcional composta por nós e por trilhões de microrganismos que coabitam nossos nichos, especialmente o trato gastrointestinal. Essa simbiose não é um detalhe periférico; ela é a base da nossa saúde física e, fundamentalmente, da nossa saúde mental. A homeostase, aquele equilíbrio que tanto buscamos na clínica, não depende exclusivamente de processos endógenos. Ela é uma conversa constante, um fluxo de informações moleculares que vem do intestino, atravessa barreiras e molda quem somos.
Nesse cenário, a psiconeuroimunologia deixa de ser uma disciplina de “setores” para se tornar um rizoma. Pense em uma rede de raízes de grama: não há um comando central único, não há uma hierarquia linear. As vias de sinalização operam em conexões múltiplas e multidirecionais. O sistema nervoso, o endócrino e o imunológico estão tão entrelaçados que as divisões acadêmicas entre eles parecem, hoje, quase artificiais. O sistema imunológico, por exemplo, precisa ser compreendido como um órgão sensorial vasto e móvel. Ele não serve apenas para nos defender de invasores; ele “sente” o estado interno e ambiental, traduzindo estímulos bioquímicos em respostas que mudam nosso comportamento e nossas emoções.
É aqui que as moléculas entram na dança. As citocinas, quimiocinas e metabólitos microbianos são os mensageiros que atravessam fronteiras teciduais. Até a barreira hematoencefálica, que antes julgávamos intransponível, revela-se agora uma interface dinâmica e permeável, permitindo que o tráfego de células e sinais altere a função sináptica e a própria plasticidade cerebral. Quando um componente periférico falha, o eco é sentido na cognição. Um exemplo vívido dessa integração é a produção de ácidos graxos de cadeia curta, como o butirato e o propionato, subprodutos da nossa microbiota. Eles não ficam restritos ao intestino; eles exercem efeitos epigenéticos, inibindo enzimas e influenciando a transcrição de genes ligados à neuroproteção. Por outro lado, se o estado inflamatório sistêmico se eleva, o corpo desvia o metabolismo do triptofano — que deveria virar serotonina — para a via das cinureninas, gerando metabólitos que afetam diretamente o humor. É a biologia explicando por que uma inflamação que começa longe do crânio pode terminar em um quadro de depressão ou ansiedade.
A alteração em um componente periférico repercute em processos cognitivos e emocionais, evidenciando a interdependência entre a saúde metabólica e a integridade psíquica. A produção de ácidos graxos de cadeia curta, como o butirato e o propionato, exemplifica essa integração, pois esses compostos exercem efeitos epigenéticos através da inibição de histonas desacetilases, influenciando a transcrição de genes relacionados à neuroproteção e à regulação da inflamação. A via das cinureninas, derivada do metabolismo do triptofano, representa outro ponto de convergência onde a ativação imunológica desvia a síntese de serotonina para a produção de metabólitos neuroativos, demonstrando como o estado inflamatório sistêmico pode induzir alterações no humor e na cognição.
A atividade das microglias, as células imunes residentes do cérebro, é constantemente modulada por sinais provenientes da periferia, integrando informações para ajustar o ambiente neuroquímico. A resposta ao estresse, mediada pelo eixo hipotálamo-pituitária-adrenal, insere-se interagindo com receptores de glicocorticoides em células imunes e alterando o perfil de secreção de citocinas, o que retroalimenta o sistema nervoso central. A análise clínica sob esta ótica exige o reconhecimento de que os transtornos mentais e neurológicos possuem raízes sistêmicas, onde a inflamação de baixo grau e a disbiose atuam como fatores etiológicos ou perpetuadores das patologias.
Até as microglias, as sentinelas residentes do cérebro, passam o dia “ouvindo” os sussurros que vêm da periferia. A resposta ao estresse, mediada pelo eixo HPA, interage com receptores em células imunes, alterando o perfil de secreção de citocinas que, por sua vez, retroalimentam o sistema nervoso. Perceba que os transtornos mentais e neurológicos deixam de ser “problemas da cabeça” para serem compreendidos como desequilíbrios de um sistema integrado, onde a inflamação de baixo grau e a disbiose são, muitas vezes, os motores que perpetuam a patologia.
O nervo vago surge aqui como a grande “superestrada” de informação desse rizoma. Cerca de 80% de suas fibras são aferentes, levando o estado das nossas vísceras diretamente ao cérebro, influenciando áreas límbicas e corticais. É essa comunicação bidirecional que garante que nossa percepção subjetiva de segurança ou ameaça seja traduzida em ajustes fisiológicos. No entanto, o estresse crônico quebra essa harmonia, dessensibilizando receptores e favorecendo quadros de neuroinflamação que interferem até na poda sináptica.
Para o clínico, o desafio é abandonar o reducionismo. Os sintomas psiquiátricos são manifestações terminais de uma rede complexa. O tratamento, portanto, precisa ser multimodal: olhar para a dieta, para o manejo do estresse e para a restauração da eubiose com o mesmo rigor com que olhamos para a farmacologia tradicional. A biologia molecular nos dá as ferramentas — os biomarcadores, a proporção de metabólitos, a compreensão da epigenética — mas é a visão do Holobionte que nos permite transformar o processo terapêutico.
A mente, afinal, não está apenas no cérebro. Ela emerge da atividade coordenada de todo esse ecossistema. Ao reconhecermos que somos um sistema biológico expandido, passamos a praticar uma medicina de precisão que é, no cerne, profundamente humanizada e sistêmica. O rizoma biológico é o que nos permite responder aos desafios do mundo como um todo coerente, e é nessa interconexão sem hierarquias que reside a nossa verdadeira capacidade de cura.
A Trama das Moléculas e a Conversa Neuroimune
Mergulhar na biologia molecular da psiconeuroimunologia exige que abandonemos, logo de início, as etiquetas rígidas que aprendemos nos manuais clássicos. Costumamos colocar neurotransmissores, hormônios e citocinas em gavetas separadas, como se cada um pertencesse a um reino isolado. Essa divisão é fruto da história das descobertas — o momento e o laboratório onde cada molécula foi batizada — e ignora a realidade funcional do corpo. Na prática, vivemos imersos em um “esperanto molecular”, uma linguagem comum onde as células, independentemente de sua origem, compartilham os mesmos receptores e as mesmas vias de sinalização.
Imagine um linfócito patrulhando a corrente sanguínea. Ele expressa, em sua superfície, receptores para neuropeptídeos e neurotransmissores. Isso significa que ele é capaz de “ouvir” e responder ao seu estado emocional e cognitivo em tempo real. De forma recíproca, neurônios e células gliais possuem receptores para citocinas e outros mediadores inflamatórios. O cérebro, portanto, atua como um órgão sensorial imunológico. Ele percebe uma ativação imune na periferia da mesma forma que percebe um som ou um toque, traduzindo esse sinal químico em alterações na neuroquímica, na plasticidade das sinapses e, inevitavelmente, no humor.
Essa comunicação bidirecional repousa sobre uma arquitetura molecular densa e não hierárquica. O fluxo de informações é contínuo. Tomemos o nervo vago como exemplo de uma ponte física essencial. Ele é a conexão direta que transporta dados do ambiente visceral e da microbiota intestinal para o tronco encefálico. As fibras aferentes vagais detectam metabólitos bacterianos e mediadores inflamatórios locais, convertendo esses sinais químicos em potenciais de ação. É um relatório constante sobre o estado imunológico periférico enviado ao comando central. Em resposta, o sistema nervoso autônomo utiliza suas vias eferentes para regular a função das células imunes, inibindo a liberação excessiva de citocinas e protegendo os tecidos de danos colaterais. Quando esse arco reflexo falha, abrimos caminho para que a inflamação de baixo grau se torne uma inquilina permanente, alimentando diversas condições neuropsiquiátricas.
Dentro dessa rede, o componente microbiano atua como uma glândula endócrina virtual. As bactérias que habitam nosso intestino sintetizam precursores de neurotransmissores, como o triptofano, e produzem ácidos graxos de cadeia curta. Compostos como o butirato e o propionato possuem a chave para atravessar a barreira hematoencefálica ou estimular células enteroendócrinas, influenciando diretamente o desenvolvimento das microglias e a mielinização dos neurônios. A maturação do nosso sistema nervoso depende, em grande medida, desses sinais exógenos que vêm dos nossos simbiontes. Se a composição dessa população bacteriana sofre uma ruptura — a disbiose — a permeabilidade das nossas barreiras biológicas se altera. Antígenos microbianos tocam o sistema imune sistêmico, desencadeando respostas inflamatórias que alcançam o parênquima cerebral.
As citocinas pró-inflamatórias, como a interleucina 1 beta (IL-1β), o fator de necrose tumoral alfa (TNF-α) e a interleucina 6 (IL-6), são os mediadores primários dessa conversa. Elas exercem efeitos que extrapolam o combate a patógenos e atingem o cerne da fisiologia neuronal. A sinalização da IL-1β no hipocampo ilustra bem esse ponto: ela interfere na plasticidade sináptica e na potenciação de longa duração, afetando mecanismos de memória e aprendizado mesmo sem qualquer lesão tecidual visível. Essas moléculas chegam ao cérebro por vias distintas, seja por transporte ativo através da barreira hematoencefálica, por difusão em áreas onde essa barreira é mais porosa — como os órgãos circunventriculares — ou pela sinalização via nervo vago.
A detecção periférica dessas citocinas pelo vago desencadeia o que chamamos de “comportamento de doença”. Trata-se de uma reorganização profunda do estado motivacional e psicomotor. O indivíduo passa a sentir anedonia, fadiga, desejo de isolamento social e alterações no sono. Embora pareçam sintomas de um transtorno mental isolado, são, na verdade, uma resposta adaptativa coordenada. O corpo economiza energia para o sistema imunológico, redirecionando recursos metabólicos e protegendo o grupo ao limitar a circulação do indivíduo possivelmente infectado. O problema surge quando esse estado se torna crônico na ausência de um patógeno, mantido por estressores psicossociais ou metabólicos.
Um dos pontos mais críticos dessa convergência é o metabolismo do triptofano. Em condições normais, o triptofano segue o caminho da síntese de serotonina, essencial para o equilíbrio do humor. No entanto, diante de citocinas inflamatórias, a enzima indoleamina 2,3-dioxigenase (IDO) é ativada, desviando o triptofano para a via da quinurenina. Aqui, o cenário se divide: nos astrócitos, produz-se o ácido quinurênico, que em excesso bloqueia receptores nicotínicos e reduz a liberação de dopamina, levando à disfunção cognitiva. Já nas microglias, o caminho leva ao ácido quinolínico, um composto neurotóxico que ativa excessivamente os receptores NMDA, gerando estresse oxidativo e excitotoxicidade. Esse desvio metabólico é o elo molecular que une uma inflamação sistêmica à neurodegeneração e aos transtornos do humor.
A regulação desse sistema também passa pelo eixo hipotálamo-pituitária-adrenal (HPA). Os glicocorticoides, como o cortisol, deveriam atuar como o freio natural da inflamação. Contudo, o estresse crônico promove a dessensibilização dos receptores de glicocorticoides. As células imunes tornam-se resistentes ao sinal de “parar”, e a resposta inflamatória prossegue sem controle. Esse ciclo vicioso compromete a resiliência do sistema, permitindo que o ruído inflamatório interfira em processos neurobiológicos fundamentais.
A sinalização purinérgica adiciona outra camada de complexidade. O ATP extracelular, liberado em situações de estresse celular, atua como uma molécula de perigo. Ele ativa receptores nas células da glia que são essenciais para a montagem do inflamassoma NLRP3. Esse complexo proteico processa a IL-1β para sua forma ativa, ligando o estresse celular diretamente à resposta imune inata dentro do cérebro. Percebam que a rede é tão integrada que neurotransmissores clássicos, como a acetilcolina, modulam a função imune através da via anti-inflamatória colinérgica. A acetilcolina, ao ligar-se a macrófagos, inibe a liberação de citocinas, mostrando como o sistema nervoso autônomo regula a intensidade da resposta imune sistêmica.
Compreender esses fundamentos transforma a prática clínica. O sintoma psiquiátrico deixa de ser um evento final e passa a ser visto como uma manifestação comportamental de uma rede em desequilíbrio. A depressão maior, os transtornos de ansiedade e o declínio cognitivo apresentam, muitas vezes, assinaturas imunológicas claras, como a elevação da proteína C-reativa e da IL-6. O desafio do especialista é aprender a ler esses fluxos moleculares, reconhecendo que a saúde emerge da harmonia entre o metabolismo, a imunidade e a ecologia microbiana. Ao silenciarmos o ruído do dualismo mente-corpo, passamos a intervir na raiz biológica da experiência humana.
A Arquitetura das Sentinelas: Do Berço Medular às Fronteiras Meningeas
Toda a complexidade da resposta imune encontra sua origem na medula óssea, partindo de células-tronco hematopoiéticas pluripotentes. Essas células representam o ponto de divergência entre duas linhagens fundamentais que se entrelaçam na manutenção da integridade orgânica: a mieloide e a linfoide. A linhagem mieloide dá origem aos neutrófilos, eosinófilos, basófilos, monócitos e células dendríticas, componentes que atuam como os primeiros sensores de perturbação ambiental. Para o clínico, a compreensão dessa linhagem é crucial, pois ela compartilha progenitores e mecanismos funcionais com a microglia, a população de macrófagos residentes do sistema nervoso central que, diferentemente dos macrófagos periféricos, coloniza o cérebro precocemente durante a embriogênese, oriunda do saco vitelino.
A maturação dessas células ocorre nos órgãos linfoides primários, onde o treinamento para a autotolerância é rigoroso. No timo, os progenitores linfoides passam por processos de seleção positiva e negativa em compartimentos histológicos distintos. No córtex tímico, a sobrevivência dos linfócitos depende da capacidade de reconhecer antígenos em um contexto de restrição molecular. Na transição para a medula tímica, a influência do gene AIRE (Autoimmune Regulator) permite que células epiteliais medulares apresentem proteínas teciduais específicas, inclusive antígenos restritos ao cérebro, como a proteína básica da mielina. Esse mecanismo garante a deleção clonal de células autorreativas antes que ganhem a circulação, estabelecendo as bases da diplomacia biológica. É fascinante notar que o timo recebe inervação autonômica e responde a flutuações de glicocorticoides, o que integra a taxa de exportação de células T virgens ao estado neuroendócrino do indivíduo.
Os órgãos linfoides secundários, como o baço e os linfonodos, funcionam como os centros de orquestração da resposta adaptativa. Nos linfonodos, a organização espacial em zonas de células T e folículos de células B permite uma interação otimizada, facilitada por células reticulares fibroblásticas que secretam quimiocinas direcionadoras. O baço exerce função análoga para antígenos de origem hematogênica, possuindo uma polpa branca organizada em bainhas linfoides periarteriais e uma polpa vermelha dedicada à filtração de eritrócitos e remoção de complexos imunes. Ambos os órgãos são densamente inervados e possuem receptores para uma ampla gama de neurotransmissores, permitindo que o sistema nervoso modifique a magnitude da resposta imune em tempo real. Uma ativação em um linfonodo regional pode induzir mudanças sistêmicas na sensibilidade de receptores em locais distantes, mediadas por eixos neuroendócrinos e pela circulação de citocinas.
A interface entre o sistema imunológico e o sistema nervoso central é guardada pela barreira hematoencefálica (BHE), uma estrutura metabólica dinâmica composta por células endoteliais unidas por junções de oclusão (tight junctions), pericitos e os pés terminais dos astrócitos. A integridade dessas junções depende de proteínas como a claudina-5 e a ocludina, cuja expressão é modulada por metabólitos da microbiota intestinal, como o butirato. Em condições de inflamação sistêmica, citocinas como o TNF-α aumentam a expressão de moléculas de adesão vascular (VCAM-1 e ICAM-1), permitindo que linfócitos e monócitos, que normalmente circulariam livremente, ancorem-se na parede do vaso e transmigrem para o parênquima cerebral. Esse processo é complementado pelos órgãos circunventriculares, regiões onde a BHE é fenestrada para permitir que o cérebro monitore diretamente a composição química do sangue.
Um avanço recente fundamental na nossa compreensão da anatomia neuroimune é a caracterização dos vasos linfáticos meníngeos. Localizados na dura-máter, esses vasos drenam fluido cefalorraquidiano, macromoléculas e células imunes do espaço subaracnóideo para os linfonodos cervicais profundos. Esta conexão física direta estabelece a via aferente da imunidade cerebral, permitindo que o sistema imune periférico monitore constantemente os antígenos presentes no cérebro. A disfunção nessa drenagem correlaciona-se ao acúmulo de proteínas tóxicas, como a beta-amiloide, evidenciando que a limpeza imunológica é um processo essencial para a saúde cognitiva.
Somado a isso, o sistema glinfático atua na depuração de resíduos metabólicos do parênquima cerebral durante o sono de ondas lentas. O fluxo de líquido cefalorraquidiano é facilitado pelos canais de aquaporina-4 nos pés astrocitários, sendo impulsionado pela pulsação arterial. A eficiência desse sistema de limpeza é diretamente influenciada pelo estado de sono e pela pressão arterial, sugerindo que variáveis fisiológicas sistêmicas regulam a concentração local de mediadores inflamatórios. Dormir, sob essa ótica técnica, configura-se como um ato de saneamento imunológico cerebral.
Por fim, o tecido linfoide associado ao intestino (GALT) representa a maior concentração de células imunes do organismo humano. As placas de Peyer, distribuídas ao longo do íleo, contêm células M especializadas na captura de antígenos luminais. No epitélio intestinal, a produção de imunoglobulina A (IgA) secretora controla a composição da microbiota, impedindo a translocação bacteriana que poderia desencadear respostas inflamatórias sistêmicas. As células imunes no intestino expressam receptores para acetilcolina e serotonina, permitindo que estímulos luminais sejam traduzidos em sinais neurais que informam o sistema nervoso central. A ativação do reflexo inflamatório vagal inibe a produção de citocinas por macrófagos residentes, demonstrando um mecanismo de controle descendente que mantém a estabilidade do holobionte. Cada componente dessa arquitetura funciona como um nódulo de uma estrutura onde a alteração em um ponto gera repercussões em todo o sistema, fundindo a biologia celular à experiência clínica
A imunidade inata constitui a base filogenética da sobrevivência, operando como um sofisticado aparelho sensorial distribuído que monitora a integridade do organismo em tempo real. Este sistema atua como a interface primária entre o meio interno e o ambiente, possuindo a capacidade de discriminar a presença de agentes infecciosos e alterações na homeostase tecidual que sinalizam perigo metabólico. A resposta imediata ancora-se na ativação de receptores de reconhecimento de padrão, conhecidos pela sigla PRRs (Pattern Recognition Receptors), que identificam estruturas conservadas em patógenos, os PAMPs (Pathogen-Associated Molecular Patterns), e sinais de estresse celular endógeno, denominados DAMPs (Damage-Associated Molecular Patterns).
Os receptores do tipo Toll, ou TLRs, exemplificam a complexidade dessa vigilância molecular. Localizados tanto na membrana plasmática quanto em compartimentos endossomais, esses sensores detectam desde lipopolissacarídeos de bactérias gram-negativas até ácidos nucleicos virais. A ligação de um ligante ao seu receptor desencadeia cascatas de sinalização intracelular que utilizam proteínas adaptadoras, como a MyD88 e a TRIF. O ápice desse processo é a translocação nuclear do fator de transcrição NF-κB, o interruptor mestre que coordena a expressão de centenas de genes envolvidos na resposta inflamatória. No sistema nervoso central, a microglia expressa uma vasta gama desses receptores, permitindo que o estresse psicológico agudo ou o trauma físico resultem na liberação de moléculas de alarme como o ATP extracelular e fragmentos de DNA mitocondrial. Essas substâncias são detectadas pelos mesmos sensores que identificariam uma invasão bacteriana, o que caracteriza o fenômeno da inflamação estéril.
Um mecanismo citoplasmático de importância central nesse cenário é o inflamassoma, com destaque para o complexo NLRP3. Ele atua como um sensor de distúrbios metabólicos e estresse oxidativo, funcionando como uma plataforma multiproteica que ativa a enzima caspase-1. A função primordial da caspase-1 é clivar as precursoras de citocinas pró-inflamatórias, especificamente a pró-interleucina 1 beta e a pró-interleucina 18, em suas formas biologicamente ativas. A secreção dessas citocinas altera a permeabilidade vascular e promove o recrutamento de leucócitos circulantes. A fase vascular da inflamação aguda envolve a vasodilatação e a expressão sequencial de moléculas de adesão, como as selectinas e integrinas, na superfície do endotélio. Esse processo permite que neutrófilos realizem o rolamento, a adesão firme e a diapedese para o interstício tecidual, onde iniciam a destruição de agressores via fagocitose ou pela liberação de armadilhas extracelulares, as NETs (Neutrophil Extracellular Traps).
A propagação desses sinais inflamatórios alcança o sistema nervoso central através de vias humorais e neurais complementares. Citocinas como a IL-1β e o TNF-α utilizam o transporte ativo através da barreira hematoencefálica ou acessam o parênquima por áreas de maior permeabilidade, como os órgãos circunventriculares. Paralelamente, o nervo vago transmite informações sobre o estado inflamatório visceral diretamente ao núcleo do trato solitário no tronco encefálico. A chegada dessas informações ao cérebro dispara o comportamento de doença, um estado caracterizado por anedonia, letargia, hipersonia e anorexia. Essa reorganização fisiológica representa uma estratégia adaptativa eficiente, pois conserva energia metabólica crítica e redireciona recursos para o suporte do sistema imunológico, além de limitar a dispersão de patógenos através do isolamento social instintivo.
O metabolismo do triptofano serve como um ponto de convergência crítico entre a resposta imune inata e a neuroquímica central. A ativação da enzima indoleamina 2,3-dioxigenase (IDO) por citocinas pró-inflamatórias desvia o triptofano da síntese de serotonina para a via da quinurenina. O acúmulo de metabólitos neurotóxicos derivados dessa via, como o ácido quinolínico, promove a excitotoxicidade ao atuar como agonista dos receptores NMDA no hipocampo e no córtex pré-frontal. Simultaneamente, a inflamação inata reduz a expressão do fator neurotrófico derivado do cérebro (BDNF), comprometendo a neurogênese e a plasticidade sináptica. O equilíbrio do sistema depende da resolução ativa da inflamação, mediada por mediadores lipídicos como as resolvinas e protectinas, que sinalizam aos macrófagos para cessarem a produção de citocinas e iniciarem a eferocitose, a limpeza dos restos celulares.
A falha nos mecanismos de contra-regulação leva à persistência do estado de alerta, onde a microglia sensibilizada adota um fenótipo primed, reagindo de forma exagerada a estímulos subsequentes. Essa hiperexcitabilidade imunológica é alimentada pela translocação de componentes bacterianos decorrentes da hiperpermeabilidade intestinal, mantendo os sensores de perigo em constante ativação. O domínio técnico desses mecanismos revela que a resposta imune inata molda o fenótipo comportamental e a trajetória de saúde, integrando sinais moleculares periféricos à função cognitiva e emocional de forma indissociável.
A descoberta da imunidade inata treinada desmantelou um dos dogmas mais rígidos da imunologia clássica: a ideia de que a memória seria uma exclusividade dos linfócitos T e B. Durante gerações, ensinamos que o sistema inato era uma barreira estática, desprovida de história e capaz apenas de reagir com a mesma cinética a cada novo insulto. A realidade molecular revela um cenário muito mais plástico, onde células da linhagem mieloide, como monócitos e macrófagos, além de células residentes como a microglia, possuem a capacidade de “aprender” com exposições prévias e armazenar informações sobre insultos passados no próprio epigenoma.
Essa memória não reside em rearranjos genéticos, mas em uma profunda reprogramação epigenética e metabólica que altera o estado de prontidão da célula. No estado virgem ou não treinado, os genes que codificam citocinas pró-inflamatórias encontram-se em uma configuração de cromatina compactada, exigindo uma sinalização robusta para que a transcrição ocorra. Quando a célula encontra um estímulo primário — que pode variar de um componente fúngico a sinais neuroendócrinos como catecolaminas e glicocorticoides liberados no estresse — ocorrem modificações químicas nas caudas das histonas, as proteínas que empacotam o DNA. Marcas específicas, como a metilação da lisina 4 da histona H3 (H3K4me1 e H3K4me3) e a acetilação da lisina 27 da histona H3 (H3K27ac), funcionam como cicatrizes moleculares que mantêm a cromatina em um estado “entreaberto”.
A persistência dessas marcas epigenéticas garante que, após a resolução do estímulo inicial, a célula retorne a um estado de repouso funcional, mas carregando um potencial de resposta amplificado. Diante de um segundo desafio, mesmo que meses ou anos depois, a maquinaria de transcrição encontra o caminho livre para acessar os genes inflamatórios. O resultado é uma produção muito mais rápida e intensa de mediadores como o TNF-α e a IL-6. Esse mecanismo, que evolutivamente conferiu vantagem de sobrevivência contra infecções recorrentes, torna-se maladaptativo no contexto do estresse psicossocial crônico. O corpo interpreta o ambiente adverso como um sinal preditivo de perigo iminente, ajustando o “termostato” imunológico para um nível de alerta máximo que corrói os tecidos ao longo das décadas.
Intrinsecamente ligado a essa mudança epigenética está o recabeamento metabólico da célula imune. A imunidade treinada depende da transição da fosforilação oxidativa para a glicólise aeróbia, um fenômeno análogo ao efeito Warburg observado em células tumorais. Essa mudança fornece a energia necessária para a rápida biossíntese de citocinas e para a manutenção das enzimas de modificação da cromatina. Metabólitos do ciclo de Krebs, como o fumarato e o succinato, acumulam-se no citoplasma e atuam como moléculas sinalizadoras. O fumarato, por exemplo, inibe diretamente as desmetilases de histonas da família KDM5, perpetuando as marcas de metilação que mantêm os genes inflamatórios acessíveis. Existe, portanto, uma interdependência absoluta entre o estado energético da célula e sua capacidade de memória.
A medula óssea desempenha o papel de arquivo central dessa trajetória biológica. Como os monócitos circulantes possuem vida curta, a persistência do fenótipo treinado por longos períodos implica que as células-tronco e progenitoras hematopoiéticas (HSPCs) foram reprogramadas na sua origem. O estresse social crônico eleva os níveis de catecolaminas que, ao ativarem receptores beta-adrenérgicos na medula, enviesam a hematopoiese para a produção aumentada de células mieloides pré-ativadas. O indivíduo traumatizado ou cronicamente estressado passa a produzir gerações de monócitos que já nascem “armados”, prontos para migrar para o cérebro ao menor sinal de perturbação.
No sistema nervoso central, o principal ator desse fenômeno é a microglia. Sendo populações de vida longa que se autorrenovam localmente, as microglias são particularmente sensíveis ao priming microglial. Insultos sofridos em janelas críticas do desenvolvimento, como infecções maternas ou estresse neonatal, induzem alterações epigenéticas duradouras. Essas células primadas podem permanecer quiescentes por anos, apresentando apenas mudanças morfológicas sutis, mas reagindo com uma explosão de citocinas neurotóxicas diante de estressores na vida adulta. Esse mecanismo oferece uma explicação molecular robusta para a vulnerabilidade a transtornos do neurodesenvolvimento e para a progressão de doenças neurodegenerativas, onde a ativação crônica do inflamassoma estabiliza o fenótipo treinado patológico.
A compreensão da imunidade treinada permite ao clínico interpretar a resistência ao tratamento sob uma nova ótica. Pacientes com depressão maior que não respondem a antidepressivos monoaminérgicos frequentemente exibem marcadores de um sistema inato que não consegue “desligar” o estado de alerta. A microglia treinada interfere na plasticidade sináptica e na neurogênese do hipocampo, tornando o parênquima cerebral refratário às intervenções farmacológicas convencionais. O reconhecimento desse endofenótipo inflamatório sugere que o sucesso terapêutico depende da capacidade de remodelar a paisagem epigenética da célula imune, integrando nutrição, sono e manejo do estresse como ferramentas de reeducação biológica. A biografia do sujeito, escrita nas marcas de suas histonas, dita a reatividade do organismo no presente e molda as possibilidades de saúde no futuro.
O Ciclo da Inflamação: Da Explosão Aguda à Busca pela Harmonia
A resposta inflamatória representa uma das sinfonias mais coordenadas da natureza. Ela começa no momento exato em que os receptores de reconhecimento de padrão, expressos em macrófagos e células dendríticas, detectam a ruptura do silêncio homeostático. Essa detecção dispara uma cascata intracelular que culmina na ativação do fator nuclear kappa B (NF-κB), o grande maestro da expressão gênica imunológica. O que observamos a seguir é a liberação de mediadores primários, como a interleucina-1 beta (IL-1β), o fator de necrose tumoral alfa (TNF-α) e a interleucina-6 (IL-6), moléculas que possuem a capacidade única de reconfigurar a fisiologia do hospedeiro em questão de minutos.
O fluxo de informações entre o local da agressão e o sistema nervoso central utiliza vias redundantes e complementares. A via neural, mediada pelo nervo vago, atua como um sistema de transmissão ultrarrápido. Terminações vagais nas vísceras possuem receptores para essas citocinas, convertendo a presença química de inflamação em sinais elétricos que alcançam o núcleo do trato solitário no tronco encefálico. Paralelamente, a via humoral transporta essas mesmas moléculas pela circulação até áreas estratégicas do cérebro. O endotélio cerebral, ao perceber esse bombardeio, responde secretando mediadores secundários, como as prostaglandinas (PGE2), diretamente no parênquima.
A chegada desses sinais ao cérebro manifesta-se clinicamente no fenômeno conhecido como comportamento de doença. Trata-se de uma estratégia evolutiva refinada para garantir a sobrevivência. O hipotálamo, alvo central da IL-1β, reajusta o termostato corporal gerando febre, o que dificulta a replicação de patógenos e otimiza a função enzimática das células imunes. Simultaneamente, o indivíduo experimenta letargia, anedonia, hipersonia e anorexia. Esses sintomas representam o esforço do organismo em conservar energia metabólica, redirecionando recursos dos músculos e da cognição para o dispendioso processo de síntese de proteínas e proliferação celular. O isolamento social, visto por essa lente técnica, funciona como um mecanismo altruísta de proteção ao grupo, limitando a disseminação de possíveis infecções.
No fígado, o comando da IL-6 altera drasticamente o perfil de síntese proteica. Observamos um aumento na produção de proteína C-reativa (PCR), fibrinogênio e ferritina, enquanto a produção de albumina e transferrina é reduzida. A PCR atua como uma opsonina, ligando-se a superfícies bacterianas e células mortas para facilitar a limpeza pelo sistema complemento. Na psiquiatria contemporânea, a medição da PCR ultrassensível tornou-se uma bússola diagnóstica, permitindo identificar pacientes cujos sintomas depressivos possuem um substrato inflamatório predominante e que tendem a responder melhor a intervenções que visem o equilíbrio imunológico.
A transição da fase explosiva para a fase de resolução é um processo ativo e tão complexo quanto o início da inflamação. A resolução não decorre apenas da dissipação passiva dos sinais de alerta; ela depende da síntese de mediadores lipídicos especializados, como as resolvinas, protectinas e maresinas. Essas moléculas sinalizam para que os macrófagos cessem a produção de citocinas destrutivas e iniciem a eferocitose, a fagocitose de neutrófilos mortos e restos teciduais. Esse reparo é essencial para restaurar a integridade das barreiras biológicas, como a mucosa intestinal e a barreira hematoencefálica, impedindo que o estado de alerta se perpetue desnecessariamente.
A saúde plena reside na robustez desses mecanismos contrarreguladores. O equilíbrio entre a agressão defensiva e a pacificação tecidual garante que o sistema imunológico cumpra seu papel sensorial e protetor sem se tornar uma fonte de dano colateral. O domínio desses ciclos moleculares permite ao clínico discernir quando a resposta inflamatória é uma aliada e quando a sua persistência sinaliza o início de uma trajetória patológica crônica.
A Cronicidade e o Desgaste Alostático
A permanência de um estado inflamatório de baixa intensidade configura o que chamamos de inflamação crônica ou meta-inflamação. Diferente da resposta aguda, que é ruidosa e resolutiva, a inflamação crônica opera no silêncio dos tecidos, representando uma falha sistêmica na resolução dos processos fisiológicos. Esse estado de vigilância ininterrupta impõe um custo metabólico elevado ao organismo, forçando uma redistribuição de recursos energéticos que deveriam ser destinados ao reparo celular e à neuroplasticidade. O resultado é a transição da homeostase para a alostase — um equilíbrio precário mantido sob estresse constante que corrói a integridade orgânica.
No nível molecular, a ativação contínua do NF-κB mantém a transcrição persistente de citocinas e moléculas de adesão, perpetuando o recrutamento de leucócitos para os tecidos. Um dos motores primários dessa persistência é a resistência aos glicocorticoides. O cortisol, liberado pelo eixo hipotálamo-pituitária-adrenal em resposta ao estresse crônico, deveria atuar como o freio natural da inflamação. No entanto, a exposição prolongada a níveis elevados desse hormônio leva à regulação negativa de seus receptores nas células imunes. As sentinelas tornam-se surdas ao comando de “parar”, permitindo que a sinalização pró-inflamatória prossiga sem os freios fisiológicos adequados.
Essa desregulação encontra eco direto no parênquima cerebral. A microglia, sensibilizada por sinais periféricos contínuos, assume um fenótipo pró-inflamatório persistente, liberando mediadores neurotóxicos e espécies reativas de oxigênio. Esse ambiente hostil compromete a sobrevivência neuronal e interfere na síntese do fator neurotrófico derivado do cérebro (BDNF), essencial para a neurogênese e para a saúde das sinapses. A inflamação crônica atua como um solvente biológico, desgastando silenciosamente a arquitetura dos circuitos neurais de recompensa e motivação.
Um dos elos mais fascinantes dessa trajetória é a mudança no metabolismo energético das células imunes, fenômeno conhecido como efeito Warburg. Em estados de ativação crônica, as células abandonam a fosforilação oxidativa eficiente em favor da glicólise aeróbica rápida. Esse rearranjo metabólico garante a velocidade da resposta imune, mas priva os neurônios de um suprimento estável de glicose e nutrientes. A fadiga profunda e a lentificação cognitiva observadas em diversos quadros clínicos são, muitas vezes, o reflexo dessa crise energética celular acoplada à inflamação persistente.
O tecido adiposo visceral desempenha um papel protagonista na manutenção desse tom inflamatório. Em condições de obesidade ou síndrome metabólica, o tecido adiposo funciona como um órgão endócrino ativo e inflamado. Adipócitos hipertrofiados sofrem hipóxia e liberam adipocinas pró-inflamatórias que entram na circulação portal e sistêmica, alcançando o cérebro e contribuindo para a resistência à insulina central. Essa resistência à insulina no cérebro compromete o metabolismo da glicose neuronal e a plasticidade sináptica, sendo um fator determinante no declínio cognitivo e na depressão vascular.
A integridade das barreiras biológicas sofre as consequências desse bombardeio sistêmico. A inflamação crônica aumenta a permeabilidade intestinal, permitindo a translocação de lipopolissacarídeos bacterianos para o sangue, um fenômeno denominado endotoxemia metabólica. Esse influxo constante de padrões moleculares associados ao perigo mantém os receptores do tipo Toll (TLR4) cerebrais em estado de alerta máximo, retroalimentando a neuroinflamação. A barreira hematoencefálica, por sua vez, torna-se permeável, permitindo a infiltração de células imunes periféricas e proteínas plasmáticas tóxicas, como o fibrinogênio, que agravam a disfunção das sinapses.
A análise clínica da inflamação crônica exige que o especialista olhe para o paciente como um sistema integrado de fluxos de informação. O sintoma é o resultado final de uma rede que perdeu a capacidade de retornar ao silêncio. Intervir nesse cenário requer mais do que a simples supressão de sintomas; exige o fortalecimento das vias naturais de resolução e a restauração da eubiose intestinal e do ritmo circadiano. Ao compreendermos que a inflamação crônica é o fio condutor que une o metabolismo à fenomenologia psíquica, passamos a praticar uma medicina que trata a raiz biológica do sofrimento humano.
Linfócitos e a Cognição Imunológica
A transição da resposta inata para a adaptativa representa o salto da reação instintiva para a estratégia de alta precisão. Se o sistema inato opera com padrões moleculares ancestrais, a imunidade adaptativa introduz a dimensão do aprendizado individualizado. Os grandes protagonistas dessa fase são os linfócitos T e B, células dotadas de uma capacidade de distinção molecular que corre em paralelo à cognição neural. Enquanto o sistema nervoso processa informações através de redes sinápticas para formar memórias de conceitos e eventos, o sistema imune adaptativo utiliza a recombinação somática de genes para criar um repertório quase infinito de receptores. Esses receptores são capazes de reconhecer e “lembrar” a forma química de qualquer estrutura, seja ela um vírus invasor ou, em cenários de falha, uma proteína do próprio cérebro.
A ativação de um linfócito T virgem ocorre em um cenário de diálogo molecular crítico. A sinapse imunológica, estrutura dinâmica que espelha em complexidade a sinapse neuronal, forma-se quando uma célula apresentadora de antígeno exibe fragmentos peptídicos acoplados às moléculas do Complexo Principal de Histocompatibilidade (MHC). O reconhecimento desse complexo pelo receptor de célula T (TCR) dispara uma cascata de sinalização intracelular que envolve a fosforilação de resíduos de tirosina e o aumento do cálcio citosólico. Esse processo é energeticamente dispendioso e estritamente regulado pelo microambiente hormonal. Linfócitos expressam receptores para dopamina, serotonina e acetilcolina, o que permite ao estado psicossocial e ao tônus autonômico modularem a eficiência da resposta. Em situações de estresse agudo, a liberação de noradrenalina pode suprimir a proliferação linfocitária, um mecanismo evolutivo voltado para a conservação de energia durante a resposta de luta ou fuga.
Os linfócitos T CD4 auxiliares, ou helpers, atuam como os regentes dessa orquestra. Dependendo do perfil de citocinas presente no momento da ativação, eles se diferenciam em linhagens funcionais distintas que determinam a natureza da inflamação. A polarização Th1, induzida pela interleucina-12, foca na defesa contra patógenos intracelulares através da produção de interferon-gama. Embora essencial para a vigilância antiviral, a atividade Th1 excessiva associa-se a processos neuroinflamatórios que afetam a integridade da barreira hematoencefálica. Por outro lado, o eixo Th17, produtor de IL-17, possui um papel determinante na manutenção das barreiras mucosas, mas sua infiltração no sistema nervoso central tem sido implicada na fisiopatologia de doenças desmielinizantes e em estados depressivos graves. A IL-17 altera a expressão de proteínas de junção oclusiva nas células endoteliais cerebrais, facilitando a entrada de leucócitos no parênquima e criando um ambiente de vulnerabilidade neurobiológica.
A imunidade mediada pelos linfócitos B complementa essa rede através da produção de imunoglobulinas e da secreção de citocinas moduladoras. Reconhecemos hoje que os linfócitos B são apresentadores de antígenos extremamente eficientes, influenciando diretamente o destino das células T. A produção de anticorpos de alta afinidade, como a IgG sistêmica e a IgA secretora, é moldada pelo contexto neuroendócrino. A presença de receptores para neuropeptídeos nos linfócitos B, incluindo a substância P e o peptídeo intestinal vasoativo, permite que o sistema nervoso module a magnitude da resposta humoral. A descoberta de autoanticorpos neuronais, como os dirigidos contra o receptor NMDA (anti-NMDAR), revolucionou a interface entre neurologia e psiquiatria. Esses anticorpos podem causar a internalização de receptores sinápticos, induzindo quadros de psicose aguda, catatonia e déficits de memória que mimetizam transtornos psiquiátricos primários. A reversibilidade desses sintomas após a remoção dos anticorpos prova que muitas patologias da mente são funcionais e mediadas pela imunidade adaptativa, e não necessariamente o resultado de processos degenerativos estruturais.
Linfócitos T e B patrulham regularmente os espaços meníngeos e o plexo coroide, exercendo uma vigilância necessária para a função cognitiva normal. Citocinas derivadas de células T, como a IL-4, promovem a expressão de fatores neurotróficos por astrócitos e neurônios, favorecendo a aprendizagem e a consolidação da memória. A interrupção dessa sinalização resulta em déficits cognitivos, evidenciando que a competência imunológica é um pré-requisito para a sanidade. O fluxo de informações é bidirecional e constante: estados mentais influenciam a taxa de proliferação linfocitária, enquanto a atividade dessas células molda a percepção, o comportamento e a própria identidade biológica do indivíduo.
Tolerância Imunológica e Resiliência Psíquica
A vitalidade de um organismo depende de uma premissa biológica fundamental e silenciosa: a capacidade do sistema imunológico de não reagir. A tolerância imunológica representa um processo ativo, energicamente custoso e finamente orquestrado para prevenir a autodestruição. Em um sistema onde a distinção entre o “eu” e o “outro” é fluida e funcionalmente integrada, a tolerância atua como o mecanismo diplomático que permite a coexistência simbiótica. Para o clínico, o estudo da tolerância é essencial, pois sua ruptura constitui o evento central na patogênese das doenças autoimunes e, conforme evidências robustas sugerem, desempenha um papel determinante na resiliência ao estresse e na manutenção da homeostase psíquica.
O estabelecimento da tolerância ocorre em dois níveis anatômicos e temporais distintos. A tolerância central opera nos órgãos linfoides primários durante o desenvolvimento celular. No timo, células epiteliais especializadas expressam o fator de transcrição AIRE, que permite a apresentação de proteínas específicas de tecidos periféricos, incluindo antígenos restritos ao cérebro, como a proteína básica da mielina. Timócitos imaturos que reconhecem esses autoantígenos com alta afinidade recebem sinais de morte por apoptose. Esse processo ensina o sistema imune a ignorar os próprios tecidos antes mesmo que as células ganhem a circulação. No entanto, essa seleção não é perfeita, e linfócitos autorreativos que escapam desse filtro precisam ser contidos pela tolerância periférica.
A regulação ativa mediada por linfócitos T reguladores (Tregs) constitui o pilar mais dinâmico da tolerância nos tecidos. Caracterizadas pela expressão do fator de transcrição FoxP3, as células Treg suprimem a ativação excessiva de outros clones e secretam citocinas anti-inflamatórias potentes, como a IL-10 e o fator de crescimento transformador beta (TGF-beta). O TGF-beta possui propriedades neurotróficas e participa da regulação da ativação microglial, conectando a paz imunológica à saúde neuronal. A psiquiatria biológica identifica a falha nessa regulação como um componente da depressão maior e do transtorno de estresse pós-traumático. Pacientes com esses quadros frequentemente exibem uma redução numérica ou funcional das células Treg, criando um ambiente permissivo para a inflamação sistêmica e neural.
O eixo hipotálamo-pituitária-adrenal atua como o maestro dessa orquestração. O cortisol exerce um efeito tolerogênico sistêmico ao induzir a apoptose de linfócitos autorreativos e promover a diferenciação de macrófagos para o perfil reparador M2, que favorece a geração de novas Tregs. O paradoxo do estresse crônico reside na resistência aos glicocorticoides: a exposição contínua a níveis elevados de cortisol leva à regulação negativa de seus receptores nas células imunes. O resultado é um sistema que opera sem os freios endócrinos naturais, rompendo a tolerância e explicando a alta comorbidade entre o sofrimento psíquico prolongado e o desenvolvimento de patologias autoimunes.
A microbiota intestinal atua como o grande educador periférico desse equilíbrio. O intestino é a maior superfície de contato com antígenos estranhos, e a decisão de tolerar simbiontes e alimentos, mantendo a vigilância contra patógenos, é mediada pela indução de Tregs no tecido linfoide associado ao intestino. Metabólitos bacterianos, especialmente o butirato, são potentes indutores da expressão de FoxP3. Células Treg “educadas” no ambiente intestinal circulam sistemicamente e migram para o sistema nervoso central, onde controlam a neuroinflamação. A disbiose compromete esse “banco” de células reguladoras, facilitando a emergência de autoimunidade em órgãos distantes.
Os mecanismos de checkpoint imunológico, como as moléculas CTLA-4 e PD-1, funcionam como freios moleculares que impedem ataques inadvertidos ao sistema nervoso. A importância desses mecanismos tornou-se evidente na oncologia moderna, onde o uso de inibidores de checkpoint para liberar o ataque imune contra tumores resulta, por vezes, em efeitos colaterais como encefalites e psicose autoimune. Isso confirma que clones autorreativos estão presentes de forma latente em indivíduos saudáveis, sendo mantidos sob controle apenas por esses mecanismos regulatórios ativos.
A saúde mental pode ser interpretada como um estado de tolerância imunológica bem-sucedida. A capacidade do sistema de “perdoar” estímulos inócuos e conter a inflamação preserva o tecido neural de ataques colaterais e garante a plasticidade necessária para a adaptação. A transição da vigilância persistente para a resiliência imunológica é o objetivo fundamental na gestão do paciente. Ao compreendermos que o silêncio imunológico não é inatividade, mas uma vigilância refinada e diplomática, passamos a valorizar intervenções que reensinem o organismo a tolerar, restaurando a harmonia entre o eu biológico e o mundo que o cerca.
A Tríade Intestino-Cérebro-Imunidade
A compreensão da individualidade biológica na medicina contemporânea repousa sobre a integração funcional entre o genoma do hospedeiro e o microbioma. No campo da psiconeuroimunologia, o eixo intestino-cérebro configura-se como uma rede de sinalização multidirecional extremamente complexa, onde o sistema imunológico atua como o principal mediador de informações entre o ambiente luminal entérico e o parênquima cerebral. Essa configuração retira do cérebro a exclusividade do comando, distribuindo o processamento de dados por múltiplos nós que incluem o sistema nervoso entérico, as populações microbianas e o tecido linfoide associado à mucosa. A comunicação entre esses componentes processa-se por meio de um fluxo ininterrupto de metabólitos, citocinas e neurotransmissores que regulam a homeostase fisiológica e os processos cognitivos de forma simultânea.
A barreira intestinal funciona como a interface primária dessa interação, sendo densamente povoada por células imunitárias que monitoram a composição da microbiota. Receptores de reconhecimento de padrão, como os do tipo Toll e NOD, presentes nas células epiteliais e dendríticas, identificam sinais de perigo ou de simbiose. A ativação desses sensores desencadeia cascatas de sinalização intracelular que resultam na produção de citocinas. Em um estado de eubiose, a microbiota comensal promove a secreção de interleucina-10 e a diferenciação de células T reguladoras, mantendo a tolerância e a integridade da barreira mucosa. Esse equilíbrio impede a translocação de endotoxinas para a circulação sistêmica, protegendo o sistema nervoso central de respostas inflamatórias de baixa intensidade que poderiam comprometer a função neuronal.
A integridade dessa barreira depende fundamentalmente de proteínas de junção oclusiva, cuja expressão é regulada por metabólitos bacterianos, com destaque para os ácidos graxos de cadeia curta. O butirato, produzido pela fermentação de fibras dietéticas, atua como um potente inibidor das histonas desacetilases, exercendo efeitos epigenéticos que fortalecem as junções intercelulares e modulam a resposta imune local. Além de sua função estrutural no epitélio, o butirato e o propionato ingressam na circulação sistêmica e atravessam a barreira hematoencefálica, influenciando diretamente a maturação e a função das células da microglia. A microglia depende desses sinais periféricos para manter sua capacidade de resposta a insultos neurotóxicos e sua eficiência na poda sináptica.
O metabolismo do triptofano constitui outro ponto de convergência bioquímica essencial. Em condições de eubiose, a maior parte do triptofano é utilizada para a síntese de serotonina, tanto no intestino quanto no cérebro. No entanto, a inflamação sistêmica induzida por disbiose ativa a enzima indoleamina 2,3-dioxigenase (IDO), desviando o metabolismo para a via da quinurenina. O acúmulo de ácido quinolínico decorrente desse desvio promove a excitotoxicidade glutamatérgica no hipocampo, enquanto a redução da disponibilidade de serotonina afeta o humor e a motivação. A microbiota regula esse equilíbrio, influenciando a neuroquímica central a partir da atividade metabólica periférica.
A via neural de comunicação entre o intestino e o cérebro é mediada de forma predominante pelo nervo vago. As fibras aferentes vagais expressam receptores para citocinas, hormônios intestinais e metabólitos microbianos, permitindo ao cérebro monitorar o estado metabólico do trato digestório em tempo real. A sinalização vagal exerce um efeito anti-inflamatório sistêmico por meio do reflexo inflamatório, onde a ativação de fibras eferentes colinérgicas inibe a produção de citocinas por macrófagos. Esse mecanismo evidencia a interdependência entre os sistemas nervoso e imune na preservação da estabilidade orgânica.
No contexto das patologias, a doença de Parkinson oferece uma evidência robusta da origem entérica de condições neurológicas. A hipótese de Braak postula que a agregação da alfa-sinucleína pode começar nos neurônios do plexo mioentérico em resposta a toxinas microbianas ou inflamação local. Essa proteína malovelada propagar-se-ia de forma retrógrada através do nervo vago até atingir o tronco encefálico e a substância negra. De forma semelhante, no transtorno do espectro autista, observa-se frequentemente uma disbiose que precede ou acompanha os sintomas comportamentais, onde metabólitos bacterianos anormais, como o ácido propiônico em excesso, afetam a conectividade neural e o comportamento social. O intestino, portanto, atua como um órgão endócrino e imunológico adicional, cujas oscilações moldam a biologia da mente ao longo de toda a vida.
Inflammaging e a Senescência do Sistema Imune
O envelhecimento biológico manifesta-se no sistema imunológico através de um fenômeno paradoxal conhecido como inflammaging. Trata-se do aumento progressivo do status pró-inflamatório basal do organismo, que ocorre simultaneamente ao declínio na competência da imunidade adaptativa, a imunossenescência. Diferente da inflamação aguda, a meta-inflamação associada à idade é uma combustão lenta e estéril que corrói a integridade orgânica no silêncio dos tecidos. Para o especialista, este processo constitui o substrato biológico invisível sobre o qual se assentam a neurodegeneração, o declínio cognitivo e os transtornos de humor resistentes na velhice.
A senescência celular representa o motor molecular desse declínio. Quando as células sofrem danos irreparáveis ao DNA ou estresse oxidativo intenso, elas entram em um estado de parada irreversível do ciclo celular, tornando-se metabolicamente ativas, mas funcionalmente alteradas. Essas células adquirem o Fenótipo Secretor Associado à Senescência (SASP), caracterizado pela secreção contínua de citocinas inflamatórias, como IL-6 e IL-1β, quimiocinas e proteases. Com o tempo, a eficiência do sistema imune em limpar essas células diminui, levando ao seu acúmulo nos tecidos. No cérebro, astrócitos e microglias senescentes transformam-se em fontes crônicas de neuroinflamação, contaminando as células vizinhas e perturbando a rede neural local.
A disfunção mitocondrial amplifica esse estado inflamatório. As mitocôndrias, como descendentes ancestrais de bactérias, possuem DNA e componentes de membrana que são reconhecidos como padrões moleculares de perigo se liberados no citoplasma. Com o envelhecimento, a falha nos mecanismos de mitofagia resulta no acúmulo de mitocôndrias disfuncionais que vazam DNA mitocondrial. Esse material ativa o sensor citosólico cGAS-STING e o inflamassoma NLRP3, desencadeando respostas inflamatórias estéreis de dentro da própria célula. A fadiga crônica e a lentificação psicomotora observadas na depressão geriátrica são frequentemente reflexos dessa crise energética celular acoplada à inflamação.
O tecido adiposo visceral assume um papel central na manutenção do tom inflamatório sistêmico durante o envelhecimento. Adipócitos hipertrofiados, comuns na obesidade e na síndrome metabólica, sofrem hipóxia e morte celular, recrutando macrófagos que secretam um coquetel de citocinas. Esse efluente inflamatório atinge o cérebro e contribui para a resistência à insulina central, um estado por vezes denominado “diabetes tipo 3”. A sinalização deficiente da insulina no sistema nervoso central compromete a depuração de peptídeos como a beta-amiloide e promove a hiperfosforilação da proteína tau, acelerando a trajetória rumo à doença de Alzheimer.
A barreira hematoencefálica sofre erosão contínua sob o bombardeio do inflammaging. A perda de pericitos e a disfunção das células endoteliais permitem o extravasamento de proteínas plasmáticas tóxicas, como o fibrinogênio, para o parênquima cerebral. O fibrinogênio ativa a microglia e promove a retração de espinhas dendríticas, prejudicando a plasticidade sináptica. A detecção de hiperintensidades de substância branca em exames de imagem reflete essa patologia microvascular inflamatória, servindo como um biomarcador do impacto do envelhecimento imunológico na integridade cerebral.
A involução tímica completa o cenário da imunossenescência ao reduzir a produção de novos linfócitos T virgens. O repertório imunológico torna-se progressivamente estreito, preenchido por clones de memória exaustos e específicos para infecções latentes. Essas células T senescentes perdem a expressão de moléculas coestimuladoras e passam a secretar níveis elevados de interferon-gama e TNF-alfa, alimentando o pool inflamatório sistêmico. A redução na diversidade do sistema de defesa diminui a resiliência diante de novos desafios antigênicos e aumenta o risco de autoimunidade devido à falha na regulação exercida pelas células Treg.
O envelhecimento, portanto, não deve ser compreendido como um processo isolado de desgaste mecânico, mas como uma perda progressiva da harmonia comunicacional entre os sistemas. A inflamação crônica atua como o ruído que interfere nessa conversa vital. Tratar a mente no envelhecimento exige silenciar esse ruído inflamatório, permitindo que a plasticidade residual do sistema nervoso se manifeste. Ao reconhecermos que a artrite, o diabetes, a depressão e a demência compartilham a mesma trajetória fisiopatológica de declínio sistêmico, passamos a praticar uma medicina que busca restaurar a capacidade de resolução e a vigilância eficiente, preservando a dignidade biológica e existencial do indivíduo.
O Exposoma e a Resposta Molecular ao Mundo
A definição de ambiente na medicina contemporânea expandiu-se para englobar o conceito de exposoma. Trata-se da totalidade das exposições a que um indivíduo é submetido desde a concepção até a finitude. O sistema imunológico atua como o principal sensor biológico desse conjunto de estímulos, integrando sinais físicos, como a poluição e a radiação, a sinais químicos derivados da dieta e do uso de medicamentos, e, fundamentalmente, a estímulos psicossociais. Observamos que a imunocompetência flutua continuamente, sendo recalibrada pela qualidade da interação do organismo com o seu entorno.
Os estressores psicossociais crônicos exercem um impacto profundo sobre a imunidade celular, que é o braço do sistema responsável pela defesa contra vírus e pela vigilância antitumoral. A ativação persistente do eixo hipotálamo-pituitária-adrenal (HPA) e do sistema nervoso simpático constitui a via final comum dessa interação. Quando a percepção de ameaça se torna constante, a liberação contínua de glicocorticoides e catecolaminas altera o perfil de resposta dos leucócitos. Embora o estresse agudo possa preparar o corpo para um combate iminente, a exposição crônica induz um estado de imunossupressão funcional e desregulação inflamatória.
A defesa antiviral depende criticamente da produção de interferons do tipo I e da atividade citotóxica das células Natural Killer e dos linfócitos T CD8+. O cortisol e a noradrenalina suprimem a transcrição de genes fundamentais para essa resposta. Indivíduos submetidos a isolamento social ou luto prolongado apresentam uma suscetibilidade aumentada a infecções e uma resposta vacinal diminuída. A latência viral ilustra essa conexão: vírus da família Herpesviridae estabelecem latência em gânglios sensoriais e sua reativação, manifestada em quadros como o herpes zoster ou a paralisia de Bell, frequentemente ocorre após traumas emocionais, revelando uma falha pontual na vigilância mediada pelo sistema nervoso central.
No campo da oncologia, a interação neuroimune é determinante. A vigilância tumoral exige que o sistema imune identifique e elimine células transformadas de forma eficiente. O estresse crônico inibe essa capacidade através da sinalização beta-adrenérgica direta em células tumorais e imunitárias. A ativação simpática promove a angiogênese e a metástase, ao mesmo tempo em que paralisa a citotoxicidade das células de defesa. Curiosamente, o sistema de recompensa cerebral também participa dessa rede. Estudos mostram que o estado hedônico positivo e a esperança aumentam a atividade antitumoral via inervação simpática da medula óssea. Tratar a depressão em pacientes oncológicos, portanto, é uma intervenção biológica que pode influenciar a sobrevida ao restaurar as vias neurais que dão suporte à imunidade.
Os estressores físicos do ambiente urbano interagem sinergicamente com o estresse psicológico. O material particulado fino e os gases poluentes induzem uma inflamação pulmonar que transborda para a circulação sistêmica. Partículas ultrafinas podem atingir o cérebro diretamente através do nervo olfatório, contornando a barreira hematoencefálica e agravando a neuroinflamação. A exposição acumulada a esses fatores, somada à disrupção do ritmo circadiano causada pela luz artificial noturna, desregula os relógios moleculares das células imunes. A melatonina, secretada pela glândula pineal no escuro, possui propriedades imunoestimulantes e oncostáticas que são perdidas na privação de sono crônica.
A compreensão desses mecanismos exige que o clínico investigue o ambiente de vida do paciente com o mesmo rigor que investiga os sintomas físicos. Técnicas de gerenciamento de estresse, como a meditação e a terapia cognitivo-comportamental, demonstram capacidade de reverter padrões de expressão gênica pró-inflamatórios. O exercício físico regular atua como um mimético de estresse agudo benéfico, fortalecendo a vigilância imunológica no longo prazo. O tratamento da saúde mental e a regulação do estilo de vida tornam-se, assim, pilares essenciais da prevenção oncológica e da manutenção da integridade biológica do hospedeiro.
Hipersensibilidades e a Mente Inflamada
As reações de hipersensibilidade, tradicionalmente classificadas por mecanismos moleculares e tempo de latência, devem ser compreendidas como tempestades sistêmicas que afetam invariavelmente o sistema nervoso central. A neuroinflamação alérgica representa um campo de intersecção vital, onde a ativação de vias de hipersensibilidade está intrinsecamente ligada à gênese de estados ansiosos, alterações cognitivas e perturbações do humor. O paciente atópico manifesta uma sintomatologia comportamental que reflete a irritabilidade de seu sistema imunológico, muitas vezes sendo rotulado como hipervigilante devido a esse estado de alerta biológico constante.
Os mastócitos são os protagonistas desta narrativa. Longe de serem apenas vilões em quadros de rinite ou urticária, essas células são sentinelas sofisticadas posicionadas estrategicamente nas interfaces com o ambiente e ao redor dos vasos sanguíneos cerebrais. Eles residem no tálamo, no hipotálamo e na dura-máter, onde suas funções transcendem a defesa contra parasitas. Quando um alérgeno interage com a IgE na superfície do mastócito, ocorre a degranulação explosiva. Em segundos, ocorre a liberação de uma carga de mediadores como histamina, triptase e serotonina, seguida pela síntese de novo de prostaglandinas e citocinas inflamatórias.
A histamina, mediador clássico da alergia, desempenha um papel duplo. Perifericamente, causa vasodilatação e edema. Centralmente, atua como um neurotransmissor excitatório fundamental, regulando o ciclo vigília-sono, a atenção e o controle do apetite a partir do núcleo tuberomamilar do hipotálamo. A liberação maciça de histamina periférica sinaliza para o cérebro através do nervo vago, induzindo estados de hiperexcitabilidade e ansiedade aguda. O uso de anti-histamínicos que atravessam a barreira hematoencefálica causa sedação justamente por bloquear esses receptores centrais, evidenciando a função tônica da histamina na manutenção da vigília.
A presença de mastócitos no lado cerebral da barreira hematoencefálica permite que a neuroinflamação focal ocorra mesmo sem um alérgeno físico. Estressores psicológicos agudos ativam esses mastócitos cerebrais via hormônio liberador de corticotrofina (CRH). A degranulação resultante aumenta a permeabilidade da barreira, permitindo a entrada de toxinas e células imunes periféricas no parênquima. Esse mecanismo explica a fisiopatologia da névoa cerebral e das cefaleias vasculares, posicionando o mastócito como um tradutor que converte o estresse emocional em inflamação vascular.
A imunologia das doenças atópicas, como a asma e a dermatite, é dominada pelo perfil de citocinas Th2. Existe uma correlação positiva significativa entre a presença dessas condições e o risco de depressão maior e transtornos de ansiedade. Citocinas como a IL-4 e a IL-13 influenciam negativamente a síntese de serotonina e a plasticidade sináptica. O prurido crônico na dermatite gera um estresse sensorial contínuo que esgota as reservas cognitivas e altera a arquitetura do sono, criando um ciclo vicioso de sofrimento cutâneo e psíquico. O tratamento agressivo da pele ou do pulmão configura-se, portanto, como uma medida preventiva psiquiátrica.
As hipersensibilidades alimentares mediadas por mecanismos tardios representam outra fronteira crítica. O glúten é um exemplo marcante; manifestações neuropsiquiátricas podem preceder ou até ocorrer na ausência total de sintomas intestinais. A sensibilidade ao glúten ativa receptores TLR4 no intestino, promovendo inflamação sistêmica que afeta o cérebro. Além disso, a digestão incompleta de proteínas como a gliadina e a caseína gera exorfinas com estrutura opioide. Em indivíduos vulneráveis, esses peptídeos podem atravessar as barreiras biológicas e ligar-se a receptores opioides no sistema nervoso, modulando comportamentos sociais e a percepção sensorial.
A Síndrome de Ativação Mastocitária (MCAS) manifesta o extremo dessa desregulação, com sintomas multissistêmicos recorrentes que incluem irritabilidade extrema e labilidade emocional. A identificação desses fenótipos permite intervenções que transcendem o uso de psicotrópicos convencionais, focando na estabilização da membrana dos mastócitos e na dieta. O reconhecimento de que a inflamação alérgica pode induzir comportamentos suicidas através da ativação microglial em regiões de controle do impulso reforça a gravidade dessas condições. A medicina do futuro integra essas descobertas, tratando o organismo como um sistema dinâmico de fluxos de informação onde acalmar a imunidade é o primeiro passo para acalmar a mente.
O Privilégio Imunológico e a Vigilância Cerebral
A história da imunologia manteve, durante décadas, a crença de que o sistema nervoso central operava em um isolamento absoluto, protegido por muralhas intransponíveis que o tornavam invisível ao sistema imune. A ciência contemporânea revela uma realidade muito mais sofisticada, onde o conceito de privilégio imunológico deixa de significar ausência de vigilância para representar uma forma de regulação altamente especializada e ativa. O cérebro é um órgão de baixa capacidade regenerativa, o que torna a inflamação clássica — com seu potencial destrutivo — um risco catastrófico. Por essa razão, a evolução esculpiu mecanismos que permitem a defesa e o monitoramento sem comprometer a delicada arquitetura dos circuitos neurais.
A barreira hematoencefálica atua como a primeira linha dessa regulação ativa. Ela é uma estrutura metabólica dinâmica, composta por células endoteliais unidas por junções de oclusão extremamente firmes, pericitos e os pés terminais dos astrócitos, que juntos formam a unidade neurovascular. Essas junções dependem da integridade de proteínas como a claudina-5 e a ocludina para restringir o tráfego de moléculas grandes e leucócitos. A permeabilidade dessa barreira é, contudo, modulável por sinais sistêmicos. Metabólitos da microbiota intestinal, como o butirato, são essenciais para manter a expressão dessas proteínas juncionais, evidenciando que a segurança do cérebro é mantida por sinais que emanam de órgãos distantes.
A descoberta dos vasos linfáticos meníngeos transformou nossa compreensão sobre como o sistema imune “sabe” o que ocorre dentro do crânio. Localizados na dura-máter, esses vasos drenam o fluido cefalorraquidiano e transportam antígenos e células imunes para os linfonodos cervicais profundos. Esta via estabelece um monitoramento constante, onde o sistema imune periférico é instruído, em condições de saúde, a manter um estado de tolerância em relação às proteínas cerebrais. A quebra desse protocolo de comunicação silenciosa é o que observamos em patologias como a esclerose múltipla, onde células T autorreativas conseguem infiltrar o parênquima e iniciar o ataque à bainha de mielina.
Dentro do tecido cerebral, a harmonia é mantida por uma comunicação neuroglial contínua. Neurônios saudáveis emitem sinais inibitórios, como o CD200 e a fractalcina, que se ligam a receptores na microglia para mantê-la em um estado vigilante, porém não agressivo. Astrócitos complementam essa proteção secretando citocinas anti-inflamatórias, como o TGF-beta e a IL-10. O privilégio imunológico é, portanto, um estado funcional que exige energia e coordenação constante. O sistema glinfático desempenha um papel crucial nesse saneamento, utilizando o fluxo de líquido cefalorraquidiano durante o sono para varrer detritos metabólicos e proteínas maloveladas, como a beta-amiloide. Dormir torna-se um evento imunológico vital, pois a falha nessa depuração transforma o privilégio em uma armadilha onde o lixo biológico acumulado dispara a neuroinflamação estéril.
A Desregulação Imune nas Psicopatologias
A psiquiatria biológica contemporânea fundamenta-se no reconhecimento de que os transtornos mentais representam manifestações comportamentais de desregulações sistêmicas. A inflamação, longe de ser um evento isolado, atua como um mecanismo patofisiológico central que altera a neuroquímica, a arquitetura do sono e a plasticidade das sinapses. A depressão maior constitui o modelo mais robusto para essa compreensão. Cerca de um terço dos pacientes apresenta elevações consistentes de interleucina-6 (IL-6) e proteína C-reativa, configurando um subgrupo que manifesta resistência aos antidepressivos monoaminérgicos convencionais.
O elo molecular entre a inflamação periférica e o sofrimento psíquico reside na ativação da via da quinurenina. Citocinas pró-inflamatórias induzem a expressão da enzima indoleamina 2,3-dioxigenase (IDO), que desvia o triptofano — precursor da serotonina — para a produção de metabólitos neuroativos. O ácido quinolínico, um dos produtos dessa via, atua como um potente agonista dos receptores NMDA, promovendo excitotoxicidade e atrofia neuronal em regiões críticas como o hipocampo e o córtex pré-frontal. Simultaneamente, a inflamação reduz os níveis do fator neurotrófico derivado do cérebro (BDNF), impedindo a reparação sináptica necessária para a estabilidade do humor.
Na esquizofrenia, a desregulação imune interage com o desenvolvimento do sistema nervoso. A exposição do cérebro fetal a citocinas inflamatórias, decorrente de infecções maternas durante a gestação, altera a trajetória de maturação das microglias. Essas células “primadas” tornam-se hipersensíveis, e sua reativação durante a adolescência resulta em uma poda sináptica excessiva. A eliminação exagerada de sinapses glutamatérgicas leva ao adelgaçamento cortical e à desconexão funcional característica da psicose. A descoberta de encefalites autoimunes, como a mediada por anticorpos contra o receptor NMDA, obriga a clínica a considerar a origem imunológica mesmo em quadros de psicose aguda de início súbito, onde o tratamento com imunoterapia pode levar à recuperação completa.
O transtorno bipolar apresenta uma dinâmica imunológica que acompanha a ciclicidade dos episódios de humor. Durante a mania, observamos picos de citocinas inflamatórias e marcadores de estresse oxidativo que impulsionam a liberação de dopamina e geram alta toxicidade sistêmica. A repetição desses episódios acumula o que chamamos de carga alostática, levando à neuroprogressão e ao declínio cognitivo prematuro. A disfunção mitocondrial emerge aqui como um elo central, onde mitocôndrias falhas liberam DNA mitocondrial no citosol, ativando o inflamassoma NLRP3 e perpetuando o estado inflamatório estéril.
O transtorno de estresse pós-traumático (TEPT) ilustra como o trauma psicológico se inscreve fisicamente no sistema imune. Pacientes com TEPT exibem assinaturas transcricionais de células mieloides treinadas, prontas para reagir de forma desproporcional a novos estressores. A inflamação periférica persistente sensibiliza a amígdala e o córtex cingulado anterior, dificultando a extinção de memórias traumáticas e mantendo o indivíduo em um estado de alerta hipervigilante.
A obesidade atua como um fator de amplificação nessas patologias, pois o tecido adiposo inflamado libera continuamente citocinas que atravessam a barreira hematoencefálica. Tratar a saúde mental exige, portanto, uma intervenção que alcance a raiz biológica do desequilíbrio, integrando o manejo do estresse, a nutrição e a restauração da eubiose. Ao compreendermos que a mente e o sistema imunológico aprendem e se adaptam a partir da mesma experiência biográfica, passamos a praticar uma medicina que busca não apenas silenciar sintomas, mas restaurar a harmonia de todo o ecossistema humano.
Transplantes, Rejeição e o Eixo Psiconeuroimune
A medicina de transplantes representa um dos avanços mais profundos da intervenção biomédica, pois desafia a noção fundamental de individualidade e integridade do organismo. A introdução de um órgão sólido ou de células-tronco hematopoiéticas de um doador em um receptor constitui a fusão forçada de dois ecossistemas biológicos distintos. O receptor torna-se, em termos moleculares, uma quimera, abrigando material genético, linhagens celulares e, frequentemente, a microbiota de outro ser humano. Esse evento desencadeia uma negociação complexa entre os sistemas de defesa do hospedeiro e o enxerto, um processo que é profundamente influenciado pelo estado psíquico e neurológico do paciente. A rejeição do enxerto ultrapassa o evento puramente imunológico; ela configura um fenômeno sistêmico onde o estresse, a depressão e a percepção subjetiva do órgão estranho regulam a tolerância biológica.
A base imunológica desse processo reside no reconhecimento do complexo principal de histocompatibilidade (MHC), denominado HLA em humanos. A disparidade entre os antígenos do doador e do receptor ativa a resposta alogênica, uma reação imune que envolve o reconhecimento direto e indireto de peptídeos estranhos. Linfócitos T do receptor identificam o MHC do doador, iniciando uma cascata que, sem intervenção, culminaria na destruição do tecido transplantado. No entanto, a intensidade dessa resposta varia significativamente entre indivíduos com o mesmo grau de incompatibilidade genética, evidenciando que o estado neuroendócrino desempenha um papel regulador crítico na determinação do limiar de rejeição.
O estresse psicológico atua como um potente modulador dessa resposta. O diagnóstico de falência orgânica, a espera exaustiva em listas de transplante e a complexidade da cirurgia ativam cronicamente o eixo hipotálamo-pituitária-adrenal e o sistema nervoso simpático. Embora os glicocorticoides possuam propriedades imunossupressoras agudas, a exposição prolongada e a desregulação do ritmo circadiano do cortisol levam à resistência celular. Os linfócitos T efetores tornam-se menos responsivos aos sinais de controle, enquanto a inervação simpática nos órgãos linfoides secundários libera noradrenalina, modulando a ativação e a expansão clonal das células T.
A depressão emerge como um fator de risco independente para a rejeição e a mortalidade. O perfil imunológico depressivo, marcado por níveis elevados de IL-6 e proteína C-reativa, cria um ambiente sistêmico pró-inflamatório que facilita a infiltração de células inflamatórias no enxerto. Além do mecanismo biológico direto, a saúde mental afeta drasticamente a aderência ao regime imunossupressor. A indiferença associada ao quadro depressivo leva, muitas vezes, ao abandono sutil da medicação, tornando o tratamento da depressão no transplantado uma medida vital de preservação do órgão.
O uso obrigatório de fármacos imunossupressores introduz camadas adicionais de complexidade neurológica. Os inibidores de calcineurina, como a ciclosporina e o tacrolimus, são essenciais para prevenir a rejeição, mas possuem neurotoxicidade significativa. A calcineurina é uma fosfatase abundante no tecido neural, fundamental para a função sináptica e a plasticidade. O bloqueio dessa enzima pode resultar em tremores, cefaleia e quadros confusionais agudos, como a Síndrome de Encefalopatia Posterior Reversível (PRES). Da mesma forma, os corticosteroides em doses elevadas podem induzir a “psicose esteroide”, alterando a transmissão dopaminérgica e o metabolismo da glicose cerebral.
A incorporação psicológica do órgão transplantado corre em paralelo à tolerância imunológica. O conceito de “propriedade corporal” é desafiado pela presença de uma parte física de outro ser humano. Alguns pacientes vivenciam o enxerto como um objeto intrusivo, chegando à antropomorfização do órgão e atribuindo-lhe características da personalidade do doador. A falha em integrar o órgão como parte do “eu” correlaciona-se com piores desfechos clínicos. O sistema imune responde a essa dissonância cognitiva; a aceitação psicológica plena associa-se a um melhor tônus vagal e a um perfil imunológico mais tolerogênico. O fenômeno do microquimerismo, onde células do doador migram e se estabelecem em nichos distantes como o cérebro, sugere que a tolerância é, em última análise, a aceitação de um mosaico celular que redefine a identidade do indivíduo.
A Integração Prática em Casos Clínicos
A aplicação clínica da psiconeuroimunologia exige que as manifestações patológicas sejam compreendidas como propriedades emergentes de uma rede interdependente. Ao observarmos casos complexos, a investigação deve transcender as hipóteses lineares e buscar as conexões entre a atividade inflamatória, a microbiota e a função neurocognitiva. Tomemos o exemplo de um paciente com transtorno depressivo maior resistente ao tratamento convencional. Níveis elevados de proteína C-reativa ultrassensível e de IL-6, na ausência de infecção ativa, sugerem que a sinalização inflamatória periférica está atravessando a barreira hematoencefálica. Uma vez no parênquima, essas citocinas ativam a microglia, desencadeando a via da quinurenina e o consequente acúmulo de ácido quinolínico. O resultado é a excitotoxicidade e a redução do BDNF, levando à atrofia do hipocampo observável em neuroimagem.
Nesse cenário, a depressão deixa de ser vista como um simples déficit de serotonina para ser compreendida como uma inflamação de baixo grau impulsionada, talvez, por um tecido adiposo visceral disfuncional ou por uma disbiose intestinal. O tratamento desse paciente requer o reconhecimento do componente inflamatório, sugerindo que a remissão depende tanto da modulação do estilo de vida e da dieta quanto da psicofarmacologia. O uso de inibidores seletivos de recaptação de serotonina pode ser insuficiente se a translocação de lipopolissacarídeos bacterianos continuar a ativar receptores de reconhecimento de padrões nos monócitos, perpetuando o ciclo inflamatório.
Outro panorama crítico manifesta-se na encefalite autoimune mediada por anticorpos contra o receptor NMDA. Em pacientes jovens que apresentam psicose de início súbito, discinesias orofaciais e instabilidade autonômica, a interface entre a imunidade humoral e a psique torna-se evidente. A presença de um tumor ovariano (teratoma) pode atuar como o foco antigênico inicial, levando o sistema imune a produzir anticorpos que cruzam a barreira hematoencefálica. Esses anticorpos provocam a internalização dos receptores glutamatérgicos, mimetizando os sintomas da esquizofrenia. A gravidade do quadro não se correlaciona apenas com os títulos de anticorpos, mas com a resiliência das redes neurais e a modulação endócrina concomitante. A intervenção bem-sucedida exige imunoterapia multidimensional para remover os anticorpos e restaurar a homeostase.
No contexto das doenças neurodegenerativas, como o Alzheimer, a patologia amiloide é apenas um nó de uma rede maior de desequilíbrios. Um paciente idoso com declínio cognitivo e síndrome metabólica exemplifica a integração entre metabolismo lipídico e neuroinflamação. A resistência à insulina periférica resulta na liberação de adipocinas pró-inflamatórias, que no sistema nervoso central comprometem a depuração do peptídeo beta-amiloide e promovem a hiperfosforilação da proteína tau. A análise da microbiota nesses casos frequentemente revela baixa diversidade, privando o cérebro de ácidos graxos de cadeia curta que regulam a maturação microglial. A progressão da doença é, portanto, influenciada pela saúde sistêmica do holobionte.
A dor crônica generalizada e a fibromialgia também ilustram esse modelo. A sensibilização central é mantida por uma alça de retroalimentação que envolve citocinas e a ativação de astrócitos na medula espinhal. Distúrbios do sono, comuns nesses pacientes, reduzem a eficácia dos sistemas descendentes de inibição da dor e aumentam a produção de IL-1β. A privação de sono atua como um estressor biológico que desestabiliza o ritmo circadiano do cortisol. O tratamento eficaz dessas condições envolve a modulação da microbiota e o fortalecimento do tônus vagal para reduzir a carga inflamatória sistêmica.
Cada caso clínico representa uma expressão única de uma rede biológica em constante adaptação. O reconhecimento de que o sistema imunológico funciona como um órgão sensorial que comunica o estado do corpo ao cérebro transforma a prática clínica. Os sintomas psiquiátricos e neurológicos passam a ser compreendidos como manifestações de um sistema complexo que busca manter a integridade diante de desafios multidimensionais. A eficácia terapêutica reside na capacidade de intervir de forma estratégica nessa rede, restaurando as vias de comunicação e o equilíbrio entre os diversos sistemas que compõem a unidade biológica humana.
Reprogramando as Vias da Mente
A modulação terapêutica contemporânea direciona o olhar para a regulação dos eixos moleculares que unem a periferia imunológica ao parênquima cerebral. Reconhecemos que a ativação de células imunes sistêmicas altera de forma direta a homeostase neuroquímica, o que abre caminho para intervenções baseadas em anticorpos monoclonais. O uso de agentes direcionados a citocinas pró-inflamatórias, como o TNF-α, a IL-6 e a IL-1β, exemplifica essa nova abordagem. Estudos demonstram que a redução da carga inflamatória sistêmica mitiga sintomas depressivos e déficits cognitivos em subgrupos específicos de pacientes, identificados por biomarcadores como a proteína C-reativa de alta sensibilidade. A eficácia dessas terapias depende da capacidade de estratificar o paciente não apenas pelo diagnóstico descritivo, mas pelo seu fenótipo biológico subjacente.
No nível celular, a imunoterapia avança para a modulação de vias de sinalização intracelular críticas, como a via da quinurenina. A ativação enzimática induzida por sinais inflamatórios desvia o triptofano para a produção de metabólitos neurotóxicos, como o ácido quinolínico, em detrimento da síntese de serotonina e melatonina. Intervenções que utilizam inibidores enzimáticos específicos — como os inibidores da IDO ou da KMO — buscam reequilibrar essa balança metabólica. O objetivo é reduzir a excitotoxicidade glutamatérgica e o estresse oxidativo no sistema nervoso central através de uma intervenção periférica. Essa estratégia reflete a compreensão de que processos metabólicos originados fora do crânio possuem repercussões profundas na arquitetura funcional do cérebro.
A manipulação da microbiota comensal surge como outro nó central na rede de sinalização. A aplicação de probióticos de precisão, por vezes denominados psicobióticos, e o transplante de microbiota fecal buscam restaurar a eubiose e regular a produção de metabólitos como os ácidos graxos de cadeia curta. Essas moléculas atravessam a barreira hematoencefálica ou sinalizam via nervo vago, influenciando o estado de ativação das microglias e a expressão de fatores neurotróficos. A reconfiguração do ecossistema intestinal visa a reprogramação da resposta imune inata e adaptativa, devolvendo ao sistema nervoso a resiliência necessária para enfrentar estressores ambientais.
O futuro das intervenções contempla também o ajuste fino dos checkpoints imunológicos. A utilização de moléculas como os inibidores de CTLA-4 e PD-1 fornece dados valiosos sobre a regulação da vigilância imune no sistema nervoso. A precisão dessa modulação exige o mapeamento das interações entre linfócitos T autorreativos e células gliais. No horizonte, vislumbramos o uso dessas ferramentas para potencializar a limpeza de detritos proteicos em doenças neurodegenerativas ou para suprimir respostas inflamatórias aberrantes em transtornos do humor persistentes.
A estimulação do nervo vago representa uma modalidade de imunoterapia bioeletrônica que utiliza as vias reflexas naturais para modular a liberação de citocinas. Essa intervenção demonstra como sinais elétricos podem ser convertidos em respostas bioquímicas imunomoduladoras. A ativação colinérgica eferente inibe a produção de mediadores inflamatórios por macrófagos esplênicos, estabelecendo um mecanismo de controle neural sobre a imunidade sistêmica. A integração de dispositivos vestíveis permitirá o monitoramento em tempo real desses estados, possibilitando ajustes dinâmicos nas intervenções eletrofisiológicas.
No limite da ciência atual, a nanotecnologia oferece caminhos para a entrega direcionada de agentes moduladores, permitindo a ultrapassagem da barreira hematoencefálica com maior eficiência e menor toxicidade. Nanopartículas funcionalizadas podem ser desenhadas para atingir subtipos celulares específicos, como as microglias de fenótipo reparador M2. Essa especificidade técnica respeita a complexidade das redes de sinalização e evita perturbações desnecessárias em circuitos homeostáticos preservados. A transição para uma imunoterapia de precisão depende da integração de grandes volumes de dados, transformando a prática clínica em um exercício de gestão da ecologia interna do paciente.
A Medicina da Unidade Biológica
A jornada através da psicoimunologia molecular exige a superação definitiva da separação entre mente e corpo. A compreensão contemporânea do organismo humano revela uma unidade funcional onde células eucarióticas e comunidades microbianas operam em uma rede de interdependência absoluta. Esse sistema não obedece a hierarquias lineares; ele fundamenta-se em fluxos contínuos de informação molecular que definem a saúde e a doença. No consultório, a observação do paciente passa a incluir a certeza de que a ativação do sistema imune periférico exerce efeitos diretos sobre a arquitetura neuronal e a função sináptica, ditando estados afetivos e capacidades cognitivas.
A barreira hematoencefálica atua como uma interface dinâmica e sensível, regulada pela integridade das junções oclusivas e pelo transporte seletivo de sinais. Quando essa fronteira é permeabilizada por citocinas como a IL-6 ou o TNF-α, o parênquima cerebral torna-se o palco de uma neuroinflamação de baixo grau. Esse processo altera o metabolismo do triptofano e a sinalização de neurotransmissores, contribuindo para a fisiopatologia de transtornos que antes eram vistos como puramente psíquicos. O especialista deve interpretar os sintomas não como falhas isoladas de um órgão, mas como propriedades emergentes de um sistema complexo em desequilíbrio.
A microbiota intestinal assume o papel de um órgão endócrino e imunológico central, cujos metabólitos moldam o fenótipo biológico ao longo de toda a vida. A exposição a estressores psicossociais altera essa ecologia, promovendo a translocação bacteriana e mantendo o organismo em um estado de alerta inflamatório persistente. A prática clínica futura exige ferramentas diagnósticas que integrem dados genômicos, proteômicos e metabolômicos, permitindo uma caracterização precisa do estado do paciente. Intervenções terapêuticas deverão transcender o uso exclusivo de psicofármacos, incorporando dietoterapia, regulação do ritmo circadiano e técnicas de modulação imune.
A personalização do tratamento dependerá da identificação de biomarcadores que reflitam a atividade da rede neuroimunológica em tempo real. A transição para este modelo requer que neurologistas, psiquiatras e psicólogos desenvolvam uma linguagem comum, fundamentada na biologia de sistemas e na ecologia humana. O estudo do indivíduo revela que a saúde mental está intrinsecamente ligada à resiliência imunológica, desafiando as fronteiras tradicionais das especialidades médicas. A análise da plasticidade neuronal deve ser acompanhada pela avaliação da plasticidade imunológica, reconhecendo que ambos os sistemas aprendem e se adaptam a partir da experiência biográfica do sujeito.
O monitoramento contínuo do transcriptoma de células imunes e da concentração de citocinas circulantes servirá como indicador precoce de recaídas em transtornos do humor e doenças degenerativas. A farmacogenética permitirá prever a resposta a tratamentos adjuvantes, movendo a psiquiatria da tentativa e erro para a medicina de precisão. O desafio para o profissional reside na capacidade de navegar por essa complexidade sem recorrer a reducionismos simplistas, mantendo um compromisso com uma prática tecnicamente rigorosa e profundamente humana.
A conclusão lógica deste percurso é que o tratamento do sofrimento mental é indissociável do cuidado com a integridade biológica. A ciência não encerra as perguntas, mas fornece as ferramentas para que possamos formular questões mais profundas sobre a natureza da vida. O reconhecimento de que somos ecossistemas em constante transformação redefine a ética do cuidado e a responsabilidade do especialista. A jornada científica através dos mecanismos imunopsiquiátricos culmina na certeza de que a vida se manifesta na complexidade, e a medicina mais eficaz é aquela que respeita, promove e restaura a integridade desta rede vital.


